题目内容
(8分)
Ⅰ、A和B反应生成C,假定反应刚开始只有A、B,它们的起始浓度均为1mol/L。反应进行2min后A的浓度为0.8mol/L,B的浓度为0.6mol/L,C的浓度为0.6mol/L。则在这2min内反应的平均速率VA ="_______mol/(L·" min),VB="________mol/(L·" min),VC ="________" mol/(L· min)。该反应的化学反应方程式为:___________________________。
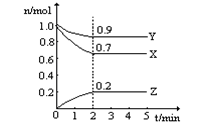
Ⅱ、某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如上图所示。根据图中数据,试填写下列空白:
(1)该反应的化学方程式为 ;
(2)从开始至2min,Z的平均反应速率为 mol/(L· min);
Ⅰ、A和B反应生成C,假定反应刚开始只有A、B,它们的起始浓度均为1mol/L。反应进行2min后A的浓度为0.8mol/L,B的浓度为0.6mol/L,C的浓度为0.6mol/L。则在这2min内反应的平均速率VA ="_______mol/(L·" min),VB="________mol/(L·" min),VC ="________" mol/(L· min)。该反应的化学反应方程式为:___________________________。

Ⅱ、某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如上图所示。根据图中数据,试填写下列空白:
(1)该反应的化学方程式为 ;
(2)从开始至2min,Z的平均反应速率为 mol/(L· min);
Ⅰ、0.1(1分) 0.2(1分) 0.3 (1分) A+2B=3C(2分)
Ⅱ、Y + 3X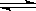 2Z (2分) 0.05 (1分)
2Z (2分) 0.05 (1分)
Ⅱ、Y + 3X
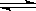 2Z (2分) 0.05 (1分)
2Z (2分) 0.05 (1分)Ⅰ、 A + B →C
C0 1 1 0
△C 0.2 0.4 0.6
C(2min)0.8 0.6 0.6
则VA=(0.2 mol/L)/2min="0.1" mol/(L· min),VB =(0.4 mol/L)/2min="0.2" mol/(L· min),
VC =(0.3 mol/L)/2min="0.3" mol/(L· min);
则VA:VB:VC =1:2:3,在同一个反应中,速率比=系数比,故反应的化学反应方程式为A+2B=3C;
Ⅱ、分析图像,得:随着时间的延长,即随着反应的进行,n(X)、n(Y)减小,则X、Y是反应物,n(z)增大,则Z为生成物;再看定量关系,X、Y、Z在2min中物质的量的变化(△n)依次为0.3 mol、0.1 mol、0.2 mol,三者的△n之比=方程式中三者的系数比,且2min后三者的物质的量均不再变化,说明达到了平衡态,即这是一个可逆反应,故方程式3X +Y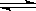 2Z;
2Z;
VZ=(0.2 mol/2L)/2min="0.05" mol/(L· min);
C0 1 1 0
△C 0.2 0.4 0.6
C(2min)0.8 0.6 0.6
则VA=(0.2 mol/L)/2min="0.1" mol/(L· min),VB =(0.4 mol/L)/2min="0.2" mol/(L· min),
VC =(0.3 mol/L)/2min="0.3" mol/(L· min);
则VA:VB:VC =1:2:3,在同一个反应中,速率比=系数比,故反应的化学反应方程式为A+2B=3C;
Ⅱ、分析图像,得:随着时间的延长,即随着反应的进行,n(X)、n(Y)减小,则X、Y是反应物,n(z)增大,则Z为生成物;再看定量关系,X、Y、Z在2min中物质的量的变化(△n)依次为0.3 mol、0.1 mol、0.2 mol,三者的△n之比=方程式中三者的系数比,且2min后三者的物质的量均不再变化,说明达到了平衡态,即这是一个可逆反应,故方程式3X +Y
 2Z;
2Z;VZ=(0.2 mol/2L)/2min="0.05" mol/(L· min);

练习册系列答案
相关题目
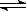 Cr(OH)3(蓝灰色)
Cr(OH)3(蓝灰色)  2SO3 (g)若经过2s后测得SO3的浓度为0.6 mol/ L,试计算:
2SO3 (g)若经过2s后测得SO3的浓度为0.6 mol/ L,试计算:
 2NH3(g) 反应,此反应达到化学平衡状态的标志是:①N2,H2和NH3的质量分数不再改变,②容器内的压强不随时间的变化而变化,③c(N2)∶c(H2)∶c(NH3)=1∶3∶2 ,④单位时间里每增加1molN2,同时增加3molH2,⑤一段时间内N2:H2:NH3的平均化学反应速率之比为1:3:2 ,⑥容器中气体的密度不变
2NH3(g) 反应,此反应达到化学平衡状态的标志是:①N2,H2和NH3的质量分数不再改变,②容器内的压强不随时间的变化而变化,③c(N2)∶c(H2)∶c(NH3)=1∶3∶2 ,④单位时间里每增加1molN2,同时增加3molH2,⑤一段时间内N2:H2:NH3的平均化学反应速率之比为1:3:2 ,⑥容器中气体的密度不变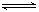 NO+SO3,当反应达平衡时,下列叙述正确的时:
NO+SO3,当反应达平衡时,下列叙述正确的时: 2NH3达到平衡的标志是( )。
2NH3达到平衡的标志是( )。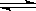 cC(g) +dD(g),C物质的质量分数(C%)与温度、压强的关系如图所示,下列判断正确的是 ( )
cC(g) +dD(g),C物质的质量分数(C%)与温度、压强的关系如图所示,下列判断正确的是 ( )