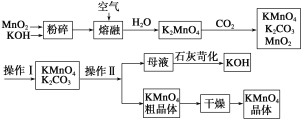
题目内容
【题目】![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 都是元素周期表中前20号主族元素,原子序数依次增大,
都是元素周期表中前20号主族元素,原子序数依次增大,![]() 是地壳中含量最高的元素,
是地壳中含量最高的元素,![]() 、
、![]() 、
、![]() 同周期,
同周期,![]() 和其他元素既不在同一周期也不在同一主族,
和其他元素既不在同一周期也不在同一主族,![]() 的氢化物及其最高价氧化物对应的水化物均为强酸,且
的氢化物及其最高价氧化物对应的水化物均为强酸,且![]() 、
、![]() 、
、![]() 的最高价氧化物对应的水化物两两混合均能发生反应生成盐和水。据此回答下列问题:
的最高价氧化物对应的水化物两两混合均能发生反应生成盐和水。据此回答下列问题:
(1)![]() 四种元素中,原子半径最大的是______(填元素符号);
四种元素中,原子半径最大的是______(填元素符号);![]() 和
和![]() 的简单氢化物中,沸点较低的是______(填化学式)。
的简单氢化物中,沸点较低的是______(填化学式)。
(2)元素![]() 在元素周期表中的位置是______,
在元素周期表中的位置是______,![]() 、
、![]() 的最高价氧化物对应的水化物之间发生反应的化学方程式为____________________________________________________________。
的最高价氧化物对应的水化物之间发生反应的化学方程式为____________________________________________________________。
(3)![]() 、
、![]() 、
、![]() 可以形成多种盐,其中一种盐中
可以形成多种盐,其中一种盐中![]() 、
、![]() 、
、![]() 三种元素的原子个数比为
三种元素的原子个数比为![]() ,该盐的化学名称为______。它的水溶液与
,该盐的化学名称为______。它的水溶液与![]() 的氢化物的水溶液反应可生成
的氢化物的水溶液反应可生成![]() 的单质,该反应的离子方程式______________________________,反应生成
的单质,该反应的离子方程式______________________________,反应生成![]() 的单质时,转移电子______
的单质时,转移电子______![]() 。
。
【答案】![]()
![]() 第3周期ⅢA族
第3周期ⅢA族 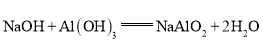 次氯酸钙
次氯酸钙 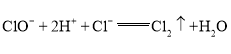 1
1
【解析】
地壳中含量最高的元素是氧,A为氧,B、C、D既然为同一周期且原子序数大于氧,那么只能是第三周期的元素,综合分析D为氯,C为铝,B只能为钠,E只能是钙,再来分析选项即可。
(1)短周期中,![]() 是除稀有气体外原子半径最大的元素,水在常温下是液体,而氯化氢在常温下是气体,因此
是除稀有气体外原子半径最大的元素,水在常温下是液体,而氯化氢在常温下是气体,因此![]() 的沸点较低;
的沸点较低;
(2)C是铝,故位于第3周期第IIIA族,写出氢氧化铝和烧碱的反应方程式![]() ;
;
(3)氯、氧、钙能形成符合描述的物质为次氯酸钙,写出次氯酸钙与氯化氢的离子方程式![]() 即可,根据离子方程式不难看出,这是氯的归中反应,因此每生成1mol氯气只需转移1mol电子。
即可,根据离子方程式不难看出,这是氯的归中反应,因此每生成1mol氯气只需转移1mol电子。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目