题目内容
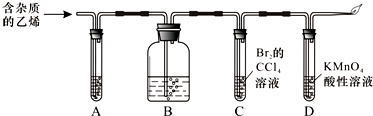
15.某课外活动小组利用如1图所示的装置进行乙醇的催化氧化实验并制取乙醛(试管丙中用水吸收产物),图中铁架台等固定装置已略去.实验时,先加热玻璃管中的铜丝,约1min后鼓入空气.请填写下列空白:
(1)检验乙醛的试剂是AC(填字母).
A.银氨溶液 B.碳酸氢钠溶液 C.新制Cu(OH)2 D.氧化铜
(2)乙醇发生催化氧化反应的化学方程式为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
(3)实验时,常常将甲装置浸在70~80℃的水浴中,目的是使生成乙醇蒸气的速率加快且较均匀,由于装置设计上的缺陷,实验进行时可能会发生倒吸.
(4)反应发生后,移去酒精灯,利用反应自身放出的热量可维持反应继续进行.进一步研究表明,鼓气速度与反应体系的温度关系曲线如图2所示.试解释鼓气速度过快,反应体系温度反而下降的原因鼓气多反应放热多,过量的气体会将体系中的热量带走,该实验中“鼓气速度”这一变量你认为可用单位时间内甲中的气泡数来估量.
(5)该课外活动小组偶然发现向溴水中加入乙醛溶液,溴水褪色.该同学为解释上述现象,提出两种猜想:①溴水将乙醛氧化为乙酸;②溴水与乙醛发生加成反应.请你设计一个简单的实验,探究哪一种猜想正确?用pH试纸检测溴水与褪色后溶液的酸碱性,若酸性明显增强,则猜想①正确;若酸性明显减弱,则猜想②正确.
分析 (1)根据乙醛中含有官能团醛基,能够发生银镜反应、能够与新制氢氧化铜溶液反应进行解答;
(2)伯醇可以被催化氧化生成醛和水,据此写出乙醇催化氧化的化学方程式;
(3)水浴加热可以让乙醇在一定的温度下成为蒸气,从而加快反应的速率;
(4)根据鼓气的速度和反应体系温度之间的关系来回答;
(5)若是乙醛被氧化,则有乙酸和溴化氢生成,溶液呈强酸性;若是发生加成反应,则生成饱和含溴有机物,溶液仍为中性,故可利用酸碱指示剂来确定哪种猜想是正确的.
解答 解:(1)乙醛分子中含有醛基,能够与银氨溶液发生银镜反应,可以用银氨溶液检验乙醛;乙醛也能够与新制的氢氧化铜浊液反应,所以可用银氨溶液或新制氢氧化铜检验乙醛,即A、C正确,
故答案为:AC;
(2)乙醇在通作催化剂时,可以被氧气氧化为乙醛,反应的方程式为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
(3)将甲装置浸在70℃~80℃的水浴中,使生成乙醇蒸气的速率加快且较均匀,导气管直接插入丙溶液内,生成的乙醛和过量的乙醇易溶于水而使丙装置产生倒吸现象,
故答案为:使生成乙醇蒸气的速率加快且较均匀;发生倒吸;
(4)反应放出的热的多少和乙醇以及氧气的量有关,鼓气多反应放热多,所以开始阶段温度升高,但是过量的气体会将体系中的热量带走,所以后阶段温度降低,实验中“鼓气速度”这一变量可通过观察甲中冒气泡的速度看出来,
故答案为:鼓气多反应放热多,过量的气体会将体系中的热量带走;单位时间内甲中的气泡数;
(5)乙醛具有还原性,乙醛被溴水氧化生成乙酸和HBr,溶液呈酸性,乙醛分子中含有不饱和键,溴水可能与乙醛发生加成反应,没有HBr生成,溶液不呈酸性,所以检验褪色后溶液的酸碱性,确定其发生哪类反应,
故答案为:用pH试纸检测溴水与褪色后溶液的酸碱性,若酸性明显增强,则猜想①正确;若酸性明显减弱,则猜想②正确.
点评 本题考查了乙醇催化氧化的实验,题目难度中等,注意掌握乙醇的组成、结构及具有的化学性质,明确乙醇催化氧化的原理,试题培养了学生的分析及化学实验能力.

| A. | 原子半径:Y>Z>R>T | |
| B. | XR2、WR2两化合物中R的化合价相同 | |
| C. | 最高价氧化物对应水化物的碱性:X>Z | |
| D. | 气态氢化物的稳定性:W<R<T |
| A. | ${\;}_{48}^{95}$Cd和${\;}_{48}^{97}$Cd互为同素异形体 | |
| B. | ${\;}_{48}^{95}$Cd和${\;}_{48}^{97}$Cd质量数相同 | |
| C. | ${\;}_{48}^{95}$Cd和${\;}_{48}^{97}$Cd是同一种核素 | |
| D. | ${\;}_{48}^{95}$Cd和${\;}_{48}^{97}$Cd互为同位素 |

| A. | 属于芳香烃 | |
| B. | 能发生取代反应和加聚反应 | |
| C. | 分子式为C15H7O | |
| D. | 不能使溴水褪色但能与氯化铁溶液发生显色反应 |
| A. | 乙烯通入酸性高锰酸钾溶液,发生取代反应 | |
| B. | 向试管中加入2mL5%硫酸铜溶液,再滴加几滴稀氢氧化钠溶液,混匀,立即加入2mL10%葡萄糖溶液,在酒精灯上加热至沸腾,可看到红色沉淀 | |
| C. | 用蒸馏法分离乙酸乙酯和饱和碳酸钠溶液 | |
| D. | 煤的干馏、煤的气化、石油裂化是化学变化,石油的分馏是物理变化 |
| A. | 过渡元素全部是金属元素 | |
| B. | 元素周期表有18个纵行,即有18个族 | |
| C. | 短周期是指第一、二、三、四周期 | |
| D. | VA族的元素全部是非金属元素 |
| A. | 将氨气通入醋酸中:NH3+H+═NH4+ | |
| B. | 在NH4Cl溶液中滴入氢氧化钠溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 将少量铜屑放入稀硝酸中:Cu+4H++NO3-═Cu2++NO↑+2H2O | |
| D. | 将稀硝酸滴在铁片上:Fe+2H+═Fe2++H2↑ |