题目内容
【题目】能正确表示下列反应的离子方程式的是( )
A.Ca(HCO3)2溶液与过量NaOH溶液反应:HCO![]() +Ca2++OH-===CaCO3↓+H2O
+Ca2++OH-===CaCO3↓+H2O
B.等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-===Mg(OH)2↓
C.铜溶于稀硝酸中:Cu+4H++2NO![]() ===Cu2++2NO2↑+2H2O
===Cu2++2NO2↑+2H2O
D.FeBr2溶液中通入少量的Cl2:2Fe2++Cl2===2Fe3++2Cl-
【答案】D
【解析】
试题分析:A.Ca(HCO3)2溶液与过量NaOH溶液反应的离子方程式为Ca2++2HCO![]() +2OH-===CaCO3↓+CO
+2OH-===CaCO3↓+CO![]() +2H2O,故A错误;B.等物质的量的MgCl2、Ba(OH)2和HCl溶液混合,先发生H++OH-=H2O的反应再生成Mg(OH)2沉淀,故B错误;C.Cu溶于稀HNO3应生成NO,故C错误;D.FeBr2溶液中通入少量的Cl2,只能氧化亚铁离子,故D正确;故选D。
+2H2O,故A错误;B.等物质的量的MgCl2、Ba(OH)2和HCl溶液混合,先发生H++OH-=H2O的反应再生成Mg(OH)2沉淀,故B错误;C.Cu溶于稀HNO3应生成NO,故C错误;D.FeBr2溶液中通入少量的Cl2,只能氧化亚铁离子,故D正确;故选D。

 名校课堂系列答案
名校课堂系列答案【题目】CO、H2、CH3、OH均是清洁能源。
(1)已知部分化学键键能数据如下:
化学键 | C | O=O | C=O | C-O |
E/(kJ mol-1) | 958.5 | 497 | 745 | 351 |
2CO(g) +O2(g)==2CO2(g) △H1
H2O(g)+CO(g)==H2(g) + CO2(g) △H2 = -41 kJmol-1
CH3OH(g)+ 3/2O2(g)==CO2(g)+2H2O(g) △H3 = -660kJmol-1
则△H1=_____ kJmol-1,反应CO(g)+2H2(g) ![]() CH3OH(g)的△H=_____ kJmol-1。
CH3OH(g)的△H=_____ kJmol-1。
(2)一定条件下,在容积为2 L的密闭容器Q中充入a mol CO与b molH2合成甲醇:CO(g) +2H2(g) ![]() CH3OH(g)。测得平衡时混合气体中CH3OH的体积百分含量与温度、 压强之间的关系如图1所示,图2表示在一定温度下,H2的平衡转化率与反应开始时两种反应物的投料物质的量之比(用X表示)、压强之间的关系。
CH3OH(g)。测得平衡时混合气体中CH3OH的体积百分含量与温度、 压强之间的关系如图1所示,图2表示在一定温度下,H2的平衡转化率与反应开始时两种反应物的投料物质的量之比(用X表示)、压强之间的关系。
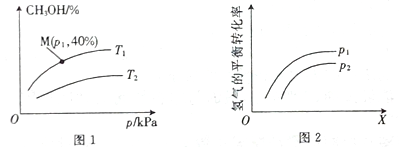
①压强相同时,温度为T1、T2时,反应达到平衡所需要的时间分别为t1、t2,则二者之间的相对大小为t1___ t2(填“>”、“<”、“=”或“无法确定”)。
②p1_____p2(填“>”、“<”、“=”或“无法确定”)。
③若a =2,b=4,则压强为p1、温度为T1时该反应的平衡常数K=______________。
④若在压强为P1、温度为T1时,向Q容器中同时加入等物质的量的CO、H2、CH3OH三种气体,则反应开始时,v(CH3OH)正_____v(CH3OH)逆(填“>”、“<”、“=”或“无法确定”)。
(3)甲醇燃料电池是一种具有高能量转化率的绿色电池,则用磷酸溶液作电解质时,负极的电极反应式为________________________。
【题目】(1)基态Fe2+离子有______个未成对电子,基态Ni原子的电子排布式为__________。
(2)用“>”或“<”填空:
第一电离能 | 熔点 | 酸性 |
Si_____S | NaCl______Si | H2SO4_____HClO4 |
(3)F2通入稀NaOH溶液中可生成OF2,OF2分子构型为_______。其中氧原子的杂化方式为_____。
(4)与H2O互为等电子体的一种阳离子为________(填化学式);
(5)Ni能与CO形成正四面体形的配合物Ni(CO)4,1mol Ni(CO)4中含有______molσ键。
(6)CaF2难溶于水,但可溶于含A13+的溶液中,原因是________(用离子方程式表示)。已知AlF63+溶液中可稳定存在。
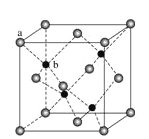
(7)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图所示,其晶胞边长为540.0 pm,密度为_______(列式并计算),a位置S2-离子与b位置Zn2+离子之问的距离为_____pm(列式表示)
【题目】除去下列物质中的杂质选用的试剂和方法最合理的是
物质 | 杂质 | 试剂 | 方法 | |
A | 甲烷 | 乙烯 | 酸性高锰酸钾溶液 | 洗气 |
B | 氯化亚铁溶液 | 氯化铁 | 过量铁粉 | 过滤 |
C | 二氧化硅 | 氧化铝 | 氢氧化钠溶液 | 过滤 |
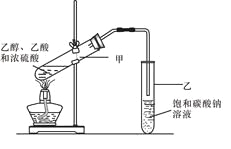
D | 乙酸乙酯 | 乙酸 | 饱和碳酸钠溶液 | 蒸馏 |
A. AB. BC. CD. D