题目内容
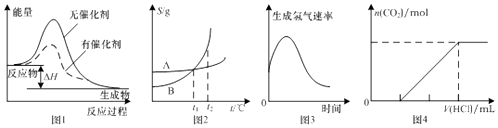
【题目】通过乙醇制取氢气通常有如下两条途径:
a.CH3CH2OH(g)+H2O(g)=4H2(g)+2CO(g)△H1=+256.6kJmol﹣1
b.2CH3CH2OH(g)+O2(g)=6H2(g)+4CO(g)△H2=+27.6kJmol﹣1
则下列说法正确的是( )
A.升高a的反应温度,乙醇的转化率增大
B.由b可知:乙醇的燃烧热为13.8 kJmol﹣1
C.2H2(g)+O2(g)=2H2O(g)△H=+485.6 kJmol﹣1
D.制取等量的氢气,途径b消耗的能量更多
【答案】A
【解析】解:A.a为吸热反应,升高温度,平衡正向移动,则乙醇的转化率增大,故A正确;B.燃烧热指应生成稳定的氧化物,应生成水、二氧化碳,故B错误;
C.氢气的燃烧为放热反应,△H<0,故C错误;
D.由热化学方程式可知生成1mol氢气,a吸收 ![]() kJ、b吸收
kJ、b吸收 ![]() kJ,故D错误.
kJ,故D错误.
故选A.
【考点精析】关于本题考查的反应热和焓变,需要了解在化学反应中放出或吸收的热量,通常叫反应热才能得出正确答案.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】研究PM 2.5、SO2、NOx等,对监测空气质量具有重要意义.取某样本用蒸馏水处理制成待测液,其中所含离子的化学组分及其浓度如下表:
离子 | K+ | Na+ | NH4+ | H+ | SO42﹣ | NO3﹣ | Cl﹣ |
浓度/molL﹣1 | 4×10﹣6 | 6×10﹣6 | 2×10﹣5 | a | 4×10﹣5 | 3×10﹣5 | 2×10﹣5 |
请回答下列问题:
(1)根据表中数据计算此待测液中c(H+)浓度a为mol/L.
(2)NOx是汽车尾气中的主要污染物之一. ①汽车发动机工作时的高温会引发N2和O2反应,反应的化学方程式是 .
②NOx能形成酸雨,由NO2形成酸雨的主要反应是(写离子方程式).
(3)为减少SO2的排放,常采取的措施有: ①在燃煤中加入生石灰可以起到固硫的作用,SO2被吸收后转化成一种硫元素的最高价态的化合物,该物质的化学式是 .
②吸收烟气中的SO2 , 以下物质可作吸收剂的是(填序号);硫酸工业中的尾气SO2可以循环利用,写出SO2转化为SO3反应的化学方程式 . a.NaOH b.H2SO4 c.NaHSO3 .