��Ŀ����
����Ŀ��2016��8�£����Ϲ������ƻ������й��������⾭��ʾ�����С��ڽ�������仧����������H2��̼���ܵȲ��������Ķ��ε�ص�ԭ����ͼ��ʾ������˵����ȷ���ǣ� �� 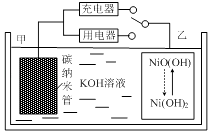
A.�ŵ�ʱ���缫Ϊ������OH�������ҵ缫
B.�ŵ�ʱ���ҵ缫��ӦΪ��NiO��OH��+H2O+e��=Ni��OH��2+OH��
C.���ʱ����ص�̼�缫��ֱ����Դ����������
D.����ܷ�ӦΪH2+2NiOOH ![]() 2Ni��OH��2
2Ni��OH��2
���𰸡�BD
���������⣺A���ŵ�ʱ���õ��Ϊԭ��أ��������Һ�����������ƶ�������OH�����缫�ƶ�����A����B���ŵ�ʱ���ҵ缫Ϊ�����õ��ӷ�����ԭ��Ӧ���缫��ӦΪ��NiO��OH��+H2O+e���TNi��OH��2+OH�� �� ��B��ȷ��
C���ŵ�ʱ��������̼�缫����������Ӧ��̼�缫�����������ʱ��̼�缫������ԭ��Ӧ��������Ӧ���Դ�ĸ�����������C����
D���ŵ�ʱ�������缫��ӦʽΪ2NiO��OH��+2H2O+2e���T2Ni��OH��2+2OH�� �� �����缫��ӦʽΪ��H2+2OH����2e���T2H2O������ʽ��ӵ��ܷ�Ӧ��H2+2NiOOH ![]() 2Ni��OH��2 �� ��D��ȷ��
2Ni��OH��2 �� ��D��ȷ��
��ѡBD��
���������õ���ʱ��ӦΪԭ���ԭ�����缫Ϊ����������������ʧ���ӷ���������Ӧ���缫��ӦʽΪH2+2OH����2e���T2H2O���ҵ缫Ϊ�����õ��ӷ�����ԭ��Ӧ���缫��ӦΪ��NiO��OH��+H2O+e���TNi��OH��2+OH�����������ӳ����ʱ��Ϊ���أ������ŵ�����෴���ݴ˽��

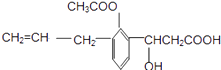
����Ŀ��ij��ѧС���Ա�����Ϊԭ�ϣ���ȡ�������������֪�й����ʵķе������
���� | �״� | ������ | ��������� |
�е�/�� | 64.7 | 249 | 199.6 |
��1���ϳɱ���������ֲ�Ʒ ��i��������λͬѧ�ֱ��������ͼ��ʾ������ʵ���Һϳɱ����������װ�ã��г������ͼ�������������ȥ���������л���ķе㣬��ò�������ס����ҡ���װ�ã������� �� 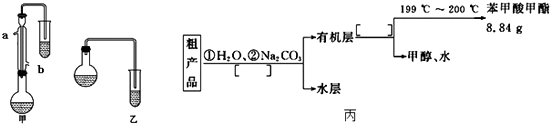
��ii��ʵ����Ũ���������������ˮӦ�����a����b������ͬ���ڽ����ڳ���
��iii����Ӧ��CH3OHӦ������������������װ���е���ĩ�˾�û�����뵽�Թ�Һ�����µ�ԭ�� ��
��2���ֲ�Ʒ�ľ��� ����������ֲ�Ʒ���������������״����������ˮ�ȣ���������������ͼ���о��ƣ���������ͼ���з�����������������������ƣ�