题目内容
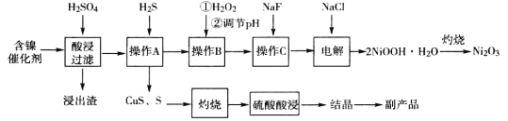
【题目】(加试题)三氧化二镍(Ni2O3)是一种灰黑色无气味有光泽的块状物,常用于制作重要的电子元件材料和蓄电池材料。某实验室尝试用工业废弃的NiO催化剂(还含有Fe2O3、CaO、CuO、BaO等杂质)为原料生产2NiOOHH2O沉淀,继而制备Ni2O3。实验工艺流程为:
已知:①有关氢氧化物开始沉淀和沉淀完全的pH如表:
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 7.2 |
沉淀完全的pH | 3.6 | 9.7 | 9.2 |
②常温下CaF2难溶于水,微溶于无机酸
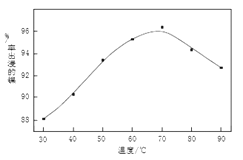
(1)操作B中需调节pH范围为____,使用Na2CO3调节pH过程中发生的反应有___。实验人员发现温度不同时,镍的浸出率不同,浸出率与温度的关系如图所示。请解释当温度高于70℃时,浸出液中Ni2+含量降低的原因____。
(2)下列说法正确的是____
A.为提高酸浸效率,可充分搅拌或适当提高硫酸浓度
B.操作A中应持续通入过量H2S气体使杂质Cu2+彻底沉淀
C.浸出渣的主要成分为CaSO42H2O和BaSO4
D.为得到副产品胆矾,应蒸发浓缩至出现大量晶体,用玻璃纤维代替滤纸进行趁热过滤
(3)电解过程中,Cl-在阳极被氧化为ClO-,但是反应前后溶液中Cl-浓度不变。写出生成沉淀反应的离子方程式_____。
(4)操作C加入NaF后如何证明沉淀完全____。
(5)工业上也可通过将草酸镍(NiC2O42H2O)在热空气中干燥脱水,再在高温下煅烧三小时制得Ni2O3,同时获得混合气体。草酸镍受热分解的化学方程式为____。
【答案】3.6~7.2 CO32-+2H+═CO2↑+2H2O,2Fe3+ +3CO32- +3H2O=2Fe(OH)3↓+3CO2↑ 温度升高,Ni2+的水解程度增大,浸出渣中Ni(OH)2含量增大,浸出率降低 AC ClO-+2Ni2++4OH-=2NiOOH·H2O↓+Cl- 静置取上层清液少许于试管中,再加入适量NaF溶液,若试管内无沉淀产生说明已经沉淀完全 2NiC2O4![]() Ni2O3+3CO↑+CO2↑
Ni2O3+3CO↑+CO2↑
【解析】
含镍催化剂与硫酸反应后Ba2+形成BaSO4沉淀,通入硫化氢气体将Cu2+沉淀,操作B除去Fe3+,操作C除去Ca2+,最后加氯化钠电解硫酸镍溶液得到2NiOOH![]() H2O↓,最终得到Ni2O3,据此分析作答。
H2O↓,最终得到Ni2O3,据此分析作答。
(1)亚铁离子不易除去,为了使铁元素被过氧化氢氧化到Fe3+并彻底除去,需调节pH至高于沉淀前的pH且低于Ni(OH)2开始沉淀的pH,防止Ni元素的损失,即pH范围为3.6~7.2;加入碳酸钠调节过程中CO32-先与酸浸时过量H+反应,再与Fe3+发生双水解生成Fe(OH)3沉淀,则离子方程式为:CO32-+2H+═CO2↑+2H2O,2Fe3+ +3CO32- +3H2O=2Fe(OH)3↓+3CO2↑;随着温度升高,镍离子的水解程度增大,浸出渣中氢氧化镍的含量增大,浸出率降低。故答案为:3.6~7.2;CO32-+2H+═CO2↑+2H2O,2Fe3+ +3CO32- +3H2O=2Fe(OH)3↓+3CO2↑;温度升高,Ni2+的水解程度增大,浸出渣中Ni(OH)2含量增大,浸出率降低;
(2)A. 充分搅拌,适当提高酸浓度的方法可以促进金属氧化物的反应,A项正确;
B.持续通入过量H2S,虽有助于Cu2+沉淀完全,但是额外消耗后续操作中添加的H2O2,造成试剂浪费,因此应通适量H2S即可,B项错误;
C. 硫酸与氧化镍、氧化铁、氧化钙、氧化铜、氧化钡分别生成硫酸盐产物,其中硫酸钡和硫酸钙难溶,因此浸出渣的主要成分为CaSO4![]() 2H2O和BaSO4,C项正确;
2H2O和BaSO4,C项正确;
D. 副产品胆矾含有结晶水,不可用蒸发结品方法分离提纯,D项错误,
故答案为:AC;
(3)Ni2+被ClO-氧化产生2NiOOH![]() H2O↓,ClO-被还原为Cl-,根据得失电子相等和电荷守恒、质量守恒配平得到ClO-+2Ni2++4OH-=2NiOOH·H2O↓+Cl-。
H2O↓,ClO-被还原为Cl-,根据得失电子相等和电荷守恒、质量守恒配平得到ClO-+2Ni2++4OH-=2NiOOH·H2O↓+Cl-。
(4)证明所有Ca2+均发生沉淀,可以静置取上层清液少许于试管中,再加入适量NaF溶液,若试管内无沉淀产生说明已经沉淀完全;
(5)草酸镍在热空气中干燥脱水后生成NiC2O4,再发生氧化还原反应,Ni由+2价升高到 +3价,则C由+3价降低到+2价,因生成混合气体,则另一气体为CO2,即生成Ni2O3、CO和CO2,再利用化合价升降相等,配平方程式为:2NiC2O4![]() Ni2O3+3CO↑+CO2↑。
Ni2O3+3CO↑+CO2↑。

 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案【题目】按要求回答下列问题:
(1)常温下向一定体积的0.1 mol/L醋酸溶液中加水稀释后,下列说法正确的是__________。
A 溶液中导电粒子的数目减少 B 醋酸的电离程度增大,c(H+)亦增大
C 溶液中c(CH3COO-)/[c(CH3COOH)c(OH-)]不变 D 溶液中c(CH3COO-)/c(H+)减小
(2)①常温下将0.15 mol/L稀硫酸V1 mL与0.1 mol/L NaOH溶液V2 mL混合,所得溶液的pH为1,则V1:V2=_____________(溶液体积变化忽略不计)。
(3)常温下,浓度均为0.lmol/L的下列五种溶液的pH值如表所示:
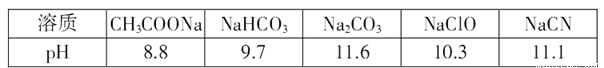
①根据表中数据,将浓度均为0.01 mol/L的下列四种酸的溶液分别稀释100倍,pH变化最小的是_____
A HCN B HClO C H2CO3 D CH3COOH
②根据以上数据,判断下列反应可以成立的是________。
A CH3COOH+Na2CO3=NaHCO3+CH3COONa B CH3COOH+NaCN=HCN+CH3COONa
C CO2 +H2O+ 2NaClO=Na2CO3+2HClO D NaHCO3+HCN=NaCN+CO2 +H2O
(4)几种离子开始沉淀时的pH如下表:
离子 | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
当向含相同浓度离子Cu2+、Fe2+、Mg2+的溶液中滴加NaOH溶液时,_________(填离子符号)先沉淀。
(5)电解质水溶液中存在电离平衡、水解平衡,请回答下列问题。
(1)已知部分弱酸的电离平衡常数如下表:
弱酸 | HCOOH | HCN | H2CO3 |
电离平衡常数(25 ℃) | Ka=1.77×10-4 | Ka=5.0×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
①同浓度HCOONa、NaCN、NaHCO3、Na2CO3这4种溶液中碱性最强的是__________;
②体积相同、c(H+