题目内容
15.下列反应能发生的是( )| A. | 氯化钠溶液和稀硫酸 | B. | 氯化钠固体和浓磷酸共热 | ||
| C. | 硝酸钠固体和浓盐酸 | D. | 亚硫酸钠固体和中等浓度硫酸 |
分析 依据复分解反应能发生的条件进行判断,两者互换成分能产生沉淀、气体或水的就能进行.
解答 解:A、氯化钠与稀硫酸不能反应生成沉淀、气体或水,故A错误;
B、氯化钠固体和浓磷酸不能反应生成沉淀、气体或水,故B错误;
C、硝酸钠和浓盐酸不能反应生成气体、沉淀或水,故C错误;
D、亚硫酸钠和稀硫酸反应生成二氧化硫气体,符合复分解发生条件,故D正确,
故选D.
点评 本题主要考查的是复分解反应发生的条件,难度不大,掌握复分解反应能发生的条件是:产生气体、沉淀或水.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
6.某有机物的结构为: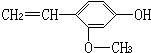 ,它不具有的性质是( )
,它不具有的性质是( )
①易溶于水 ②可以燃烧 ③能使酸性高锰酸钾溶液褪色 ④能跟KOH溶液反应 ⑤能跟NaHCO3溶液反应 ⑥能与溴水发生取代反应.
 ,它不具有的性质是( )
,它不具有的性质是( )①易溶于水 ②可以燃烧 ③能使酸性高锰酸钾溶液褪色 ④能跟KOH溶液反应 ⑤能跟NaHCO3溶液反应 ⑥能与溴水发生取代反应.
| A. | ①④ | B. | ①②⑥ | C. | ①⑤ | D. | ③⑤⑥ |
3.下列说法错误的是( )
| A. | NH4NO3溶于水吸热,说明其溶于水不是自发过程 | |
| B. | 同一物质气态时熵值最大,液态时次之,而固态时熵值最小 | |
| C. | 物质发生氧化还原反应都伴有能量转化 | |
| D. | 由能量判据和熵判据组合成的复合判据,更适合于所有的过程 |
5.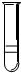 分别将5ml下列物质分别注入15ml水中,振荡后静置,能形成如图所示的是( )
分别将5ml下列物质分别注入15ml水中,振荡后静置,能形成如图所示的是( )
①溴苯②乙酸乙酯③乙醇④甘油⑤油酸甘油酯⑥硝基苯.
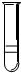 分别将5ml下列物质分别注入15ml水中,振荡后静置,能形成如图所示的是( )
分别将5ml下列物质分别注入15ml水中,振荡后静置,能形成如图所示的是( )①溴苯②乙酸乙酯③乙醇④甘油⑤油酸甘油酯⑥硝基苯.
| A. | 全部 | B. | ①②⑤⑥ | C. | ②⑤ | D. | ①⑥ |
12.下列叙述正确的是( )
| A. | 在原电池的负极和电解池的阴极上都是发生失电子的氧化反应 | |
| B. | 用惰性电极电解MgCl2溶液的反应原理:2Cl-+2H2O 电解_ Cl2↑+H2↑+2OH- | |
| C. | 用惰性电极电解稀H2SO4溶液一段时间后,溶液的酸性增强 | |
| D. | 镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
9.请回答下列问题:
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
则该元素是Al(填写元素符号).
(2)锗(Ge)可能的性质或应用有CD_.
A.是一种活泼的金属元素 B.其电负性大于硫
C.其单质可作为半导体材料 D.其最高价氯化物的沸点低于其溴化物的沸点
(3)关于化合物HOH2CCH2OH,下列叙述正确的有ABD.
A.分子间可形成氢键 B.分子中既有极性键又有非极性键
C.分子中有7个σ键和1个π键 D.该分子在水中的溶解度大于2-丁烯
(4)NaF晶体的熔点>[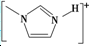 ]BF−4的熔点(填>、=或<),其原因是两者均为离子化合物,且电荷数均为1,但后者离子半径大,离子键较弱,因此熔点较低.
]BF−4的熔点(填>、=或<),其原因是两者均为离子化合物,且电荷数均为1,但后者离子半径大,离子键较弱,因此熔点较低.
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
| 电离能 | I1 | I2 | I3 | I4 | … |
| Im/kJ•mol-1 | 578 | 1 817 | 2 745 | 11 578 | … |
(2)锗(Ge)可能的性质或应用有CD_.
A.是一种活泼的金属元素 B.其电负性大于硫
C.其单质可作为半导体材料 D.其最高价氯化物的沸点低于其溴化物的沸点
(3)关于化合物HOH2CCH2OH,下列叙述正确的有ABD.
A.分子间可形成氢键 B.分子中既有极性键又有非极性键
C.分子中有7个σ键和1个π键 D.该分子在水中的溶解度大于2-丁烯
(4)NaF晶体的熔点>[
 ]BF−4的熔点(填>、=或<),其原因是两者均为离子化合物,且电荷数均为1,但后者离子半径大,离子键较弱,因此熔点较低.
]BF−4的熔点(填>、=或<),其原因是两者均为离子化合物,且电荷数均为1,但后者离子半径大,离子键较弱,因此熔点较低.  ,反应类型为取代反应.
,反应类型为取代反应.