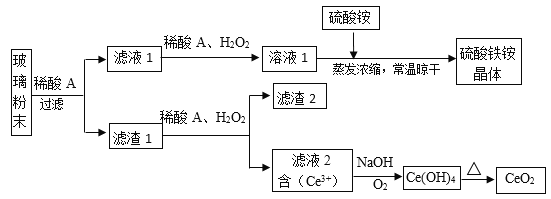
��Ŀ����
����Ŀ������N2H4����һ�ָ���ȼ�ϣ�������Ϊ��ɫ����ǿ�ҵ���ˮ�Ե��ж�Һ�塣�۵㣨2�������е㣨113.5������N2H4ˮ��Һ�ļ������ڰ�ˮ��N2H4��ǿ��ԭ�ԡ���ѧС��ͬѧ��ʵ�������ù���NH3��NaC1O��Һ��Ӧ��ȡN2H4��̽�������ʡ��ش��������⣺

��1��A�з�Ӧ����������Ϊ_____________
��2������ͼװ����ȡ�£�������˳��Ϊ________��������������Сд��ĸ��ʾ����
��3��װ��A������N2H4��H2O��������Ӧ�Ļ�ѧ����ʽΪ_________________��װ��D��������_______________��
��4���û�ѧ�������N2H4ˮ��Һ�ʼ��Ե�ԭ��__________________________________
��5��������ʱ����Ϊȼ�ϣ�˫��ˮΪ�����������߷�Ӧ���ɵ�������̬ˮ����֪1.6gҺ̬�� ��������Ӧ���ͷ�64.22kJ ��������д���÷�Ӧ���Ȼ�ѧ����ʽ��_______________________
��6����A�еõ��Ĵֲ�Ʒ���ռ��ϣ���ͨ�뵪���Գ�������Ŀ��Ϊ_______________��������Һ�¶Ƚ�110�������ռ���ȫ�ܽ����ȴ��60�����ң����� ������Һ������90%��94%���پ�����ȥˮ�ֺ��������Ƶ�98%��99��5%����ˮ�¡���հ״�Ӧ��д��_____��
A����ѹ���� B.��ѹ���� C.�������
���𰸡� ������ƿ defabc (ef˳��ɻ���) NaClO+2NH3=N2H4��H2O+NaCl ��ֹ������ȫƿ N2H4��H2O![]() N2H5++O���� N2H4��l��+2H2O2(l)=N2(g)+4H2O(g) H=-1284.4kJ/mol. ��ֹ�±��������� C
N2H5++O���� N2H4��l��+2H2O2(l)=N2(g)+4H2O(g) H=-1284.4kJ/mol. ��ֹ�±��������� C
��������������������⿼��N2H4���Ʊ���N2H4���ʵ�̽�����Ȼ�ѧ����ʽ����д��
��1�����������Ĺ����ص㣬A�з�Ӧ����������Ϊ������ƿ��
��2�����������ù���NH3��NaClO��Һ��Ӧ��ȡN2H4���������ǰ�������װ�ã���װ��C��ȡ���������ڰ�����������ˮ������NH3ֱ��ͨ��NaClO��Һ���ײ�����������Cװ�ú�����Dװ�ã�������ͨ��������ƿ����NaClO��Һ��Ӧ���£�����İ���Ҫ����β�����գ�װ�õ�����˳��ΪC��D��A��B�����������ӿڵ�����˳��Ϊdefabc��dfeabc��
��3����װ��A��NH3��������N2H4��H2O����NaClO����ԭ��NaCl����Ӧ�Ļ�ѧ����ʽΪ2NH3+NaClO=N2H4��H2O+NaCl��װ��D�����ã�����ȫƿ����������
��4�����백��ˮ��Һ�ʼ��Ե�ԭ��N2H4ˮ��Һ�ʼ��Ե�ԭ����N2H4��H2O���������룬���뷽��ʽΪ��N2H4��H2O![]() N2H5++OH-��
N2H5++OH-��
��5��n��N2H4��=![]() =0.05mol����1molN2H4��Ӧ�ų�������Ϊ
=0.05mol����1molN2H4��Ӧ�ų�������Ϊ![]() =1284.4kJ����Ӧ���Ȼ�ѧ����ʽΪN2H4��l��+2H2O2��l��=N2��g��+4H2O��g�� H=-1284.4kJ/mol��
=1284.4kJ����Ӧ���Ȼ�ѧ����ʽΪN2H4��l��+2H2O2��l��=N2��g��+4H2O��g�� H=-1284.4kJ/mol��
��6����������N2H4��ǿ��ԭ�ԣ�����ͨ��N2��������Ŀ���ǣ���ֹ�±�������������ΪN2H4�ķе�Ϊ113.5�棨����60���������Խ�����������ú�����90%~94%������Һ����ѡC��

����Ŀ����һ���¶��£�������X������Y��0.16mol����10L�����ܱ������У�������Ӧ��X�� g��+Y�� g��2Z��g����H��0��һ��ʱ���ﵽƽ�⣮��Ӧ�����вⶨ���������������˵����ȷ���ǣ�������
t�Mmin | 2 | 4 | 7 | 9 |
n��Y���Mmol | 0.12 | 0.11 | 0.10 | 0.10 |
A. ��Ӧǰ4min��ƽ����Ӧ��������Z��=0.0125molL-1min-1
B. �����������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰ�����棩����������
C. �����������䣬������ϵ�г���1L������ʹ��ϵѹǿ�����������棩����������ͬ�ȳ̶�����
D. ���¶��´˷�Ӧ��ƽ�ⳣ��K=1.44