题目内容
【题目】已知反应A(g)+B(g)![]() C(g)+D(g)。回答下列问题:
C(g)+D(g)。回答下列问题:
(1)830 ℃时,向一个5 L的密闭容器中充入0.20 mol的A和0.80 mol的B,如反应初始6 s内A的平均反应速率v(A)=0.003 mol·L-1·s-1,则6 s时c(A)=________ mol·L-1,C的物质的量为________mol;此时A的转化率为__________;反应一段时间后,达到平衡状态,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率__________。(填“增大”“不变”或“减小”)
(2)判断该反应是否达到平衡的依据为__________ (填正确选项前的字母):
a.压强不随时间改变
b.气体的密度不随时间改变
c.c(A)不随时间改变
d.单位时间里生成C和D的物质的量相等
【答案】 0.022 0.09 45% 不变 c
【解析】v(A)=0.003 mol·L-1·s-1,△c(A)= v(A)×△t=0.003 mol·L-1·s-1×6s=0.018mol/L,则6s时c(A)=(0.20mol÷5 L)-0.018mol/L= 0.022 mol/L;C的物质的量0.018mol/L×5 L= 0.09mol; 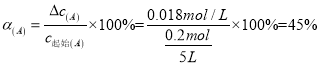 ;如果这时向该密闭容器中再充入1 mol氩气,因为容器的容积不变。A的浓度不变,所以平衡不发生移动。故平衡时A的转化率也不变。因为该反应是个反应前后气体体积相等的可逆反应,所以无论反应是否达到平衡,容器内气体的压强都不会发生改变,a项错误。由于在反应前后气体的体积不变,反应遵循质量守恒定律,质量也不变,因此任何时刻,无论反应是否达到平衡,气体的密度都不改变,b项错误;若反应未达到平衡,则 c(A)就会发生改变,现在c(A)不随时间改变,说明反应达到了平衡状态,c项正确;在方程式中,C和D都是生成物,系数相同,所以在任何时间段内单位时间里生成C和D的物质的量总是相等,因此不能以此为标准判断反应是否达到平衡状态,d项错误。
;如果这时向该密闭容器中再充入1 mol氩气,因为容器的容积不变。A的浓度不变,所以平衡不发生移动。故平衡时A的转化率也不变。因为该反应是个反应前后气体体积相等的可逆反应,所以无论反应是否达到平衡,容器内气体的压强都不会发生改变,a项错误。由于在反应前后气体的体积不变,反应遵循质量守恒定律,质量也不变,因此任何时刻,无论反应是否达到平衡,气体的密度都不改变,b项错误;若反应未达到平衡,则 c(A)就会发生改变,现在c(A)不随时间改变,说明反应达到了平衡状态,c项正确;在方程式中,C和D都是生成物,系数相同,所以在任何时间段内单位时间里生成C和D的物质的量总是相等,因此不能以此为标准判断反应是否达到平衡状态,d项错误。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案【题目】以下分离提纯操作能达到相应目的是( )
选项 | 操作 | 目的 |
A | 电解精炼 | 将粗铜转化为精铜 |
B | 蒸馏 | 分离氯化钠和硝酸钾混合溶液 |
C | 分液 | 分离乙酸与乙酸乙酯混合物 |
D | 用乙醇作萃取剂 | 提取溴水中的溴单质 |
A.A
B.B
C.C
D.D