题目内容
【题目】我国首架国产大飞机C919采用的先进材料主要有第三代铝锂合金、碳纤维复合材料及钛合金等。回答下列问题:
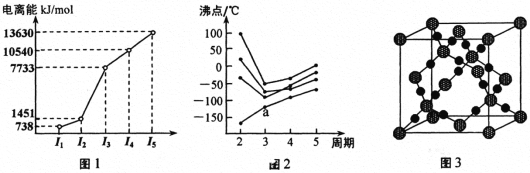
![]() 基态原子核外电子排布式为______,其核外电子占据最高能层的符号是______。
基态原子核外电子排布式为______,其核外电子占据最高能层的符号是______。
![]() 电子结合能是指在中性原子中当其他电子均处在可能的最低能态时,某电子从指定的轨道上电离时所需能量的负值。Li的2s轨道电子结合能比1s轨道的______
电子结合能是指在中性原子中当其他电子均处在可能的最低能态时,某电子从指定的轨道上电离时所需能量的负值。Li的2s轨道电子结合能比1s轨道的______![]() 填“大”或“小”
填“大”或“小”![]() ,原因是______。
,原因是______。
![]() 基碳纤维是以聚丙烯腈纤维为原料的碳纤维。丙烯腈
基碳纤维是以聚丙烯腈纤维为原料的碳纤维。丙烯腈![]() 分子中
分子中![]() 键和
键和![]() 键的个数比为______,碳原子间共价键的键角约为______。
键的个数比为______,碳原子间共价键的键角约为______。
![]() 工业上用镁还原
工业上用镁还原![]() 的方法制备金属钛,元素Mg、Ti、Cl的电负性分别为
的方法制备金属钛,元素Mg、Ti、Cl的电负性分别为![]() 、
、![]() 、
、![]() ,
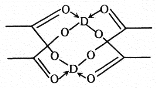
,![]() 的熔点______
的熔点______![]() 的熔点
的熔点![]() 填“高于”或“低于”
填“高于”或“低于”![]() 。
。
![]() 钛存在两种同素异构体,
钛存在两种同素异构体,![]() 采纳六方最密堆积,
采纳六方最密堆积,![]() 采纳体心立方堆积,鉴别两种钛晶体可以用______法,由
采纳体心立方堆积,鉴别两种钛晶体可以用______法,由![]() 转变为
转变为![]() 晶体体积______
晶体体积______![]() 填“膨胀”或“收缩”
填“膨胀”或“收缩”![]() 。
。
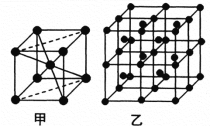
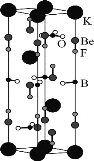
![]() 由Ba、Ti和O组成的三元离子晶体中,晶胞的顶点被
由Ba、Ti和O组成的三元离子晶体中,晶胞的顶点被![]() 占据,体心被
占据,体心被![]() 占据,面心被
占据,面心被![]() 占据,晶胞参数
占据,晶胞参数![]() ,该晶体的化学式为______。
,该晶体的化学式为______。![]() 为140pm,则
为140pm,则![]() 为______
为______![]()
【答案】![]() N 大 2s轨道上的电子离核远,能量高,电离时需要的能量少 2:1 120° 高于 X—射线衍射法 膨胀
N 大 2s轨道上的电子离核远,能量高,电离时需要的能量少 2:1 120° 高于 X—射线衍射法 膨胀 ![]()
![]()
【解析】
(1)Ti为22号元素,根据构造原理书写其电子排布式;因其核外电子所处最高能层为第四层,故最高能层符号为N;
(2)从电子结合能概念角度分析Li的2s轨道电子结合能与1s轨道结合能大小关系,重点理解电子结合能取负值;
(3)从丙烯腈分子的结构式分析,判断其σ键数目和π键数目,碳原子间共价键的键角需要分析中间C原子的杂化方式;
(4)元素Mg、Ti、Cl的电负性分别为![]() 、
、![]() 、
、![]() ,由此可知,Mg、Cl的电负性差值大于1.7,
,由此可知,Mg、Cl的电负性差值大于1.7,![]() 为离子晶体,Ti、Cl的电负性差值小于1.7,
为离子晶体,Ti、Cl的电负性差值小于1.7,![]() 为分子晶体;
为分子晶体;
(5)鉴别晶体堆积方式常用方法是X射线衍射法,αTi采纳六方最密堆积,βTi采纳体心立方堆积,由于六方最密堆积空间利用率大于体心立方堆积,故由αTi转化为βTi晶体体积膨胀;
(6)根据均摊法,计算得到晶体的化学式为BaTiO3,在该晶胞中Ba2+处在顶点位置,O2处在面心位置,面对角线长度![]() 等于2倍r(Ba2+)加上2倍r(O2),即可求出r(Ba2+)。
等于2倍r(Ba2+)加上2倍r(O2),即可求出r(Ba2+)。
![]() 为22号元素,Ti的基态原子核外电子排布式为
为22号元素,Ti的基态原子核外电子排布式为![]() ,最高能层符号为N;
,最高能层符号为N;
故答案为:![]() ;N;
;N;
![]() 电子结合能指的是在中性原子中当其他电子均处在可能的最低能态时,某电子从指定的轨道上电离时所需能量的负值,这里注意是所需能量的负值。因为Li的2s轨道上的电子离原子核比较远,能量较高,电离时需要的能量少,故2s轨道电子结合能比1s轨道的大;
电子结合能指的是在中性原子中当其他电子均处在可能的最低能态时,某电子从指定的轨道上电离时所需能量的负值,这里注意是所需能量的负值。因为Li的2s轨道上的电子离原子核比较远,能量较高,电离时需要的能量少,故2s轨道电子结合能比1s轨道的大;
故答案为:大;2s轨道上的电子离核远,能量高,电离时需要的能量少;
(3)1个丙烯腈分子中有3个C—H键、1个C=C键、1个C—C键、1个C≡N键,单键全为σ键,双键中含1个σ键和1个π键,三键中含1个σ键和2个π键,1个丙烯腈分子中含6个![]() 键和3个
键和3个![]() 键,中间的C原子采取
键,中间的C原子采取![]() 杂化,故键角为
杂化,故键角为![]() ;故答案为:2:1;
;故答案为:2:1;![]() ;
;
![]() 元素Mg、Ti、Cl的电负性分别为
元素Mg、Ti、Cl的电负性分别为![]() 、
、![]() 、
、![]() ,Cl与Mg的电负性差值为1.8>1.7,
,Cl与Mg的电负性差值为1.8>1.7,![]() 为离子晶体,Cl与Ti的电负性差值为1.5<1.7,
为离子晶体,Cl与Ti的电负性差值为1.5<1.7,![]() 为分子晶体,则
为分子晶体,则![]() 的熔点高于
的熔点高于![]() 的熔点;
的熔点;
故答案为:高于;
![]() 鉴别晶体堆积方式的方法是X—射线衍射法;六方最密堆积空间利用率比体心立方堆积空间利用率高,由
鉴别晶体堆积方式的方法是X—射线衍射法;六方最密堆积空间利用率比体心立方堆积空间利用率高,由![]() 转变为
转变为![]() 晶体体积膨胀;
晶体体积膨胀;
故答案为:X—射线衍射法;膨胀;
![]() 由结构可知
由结构可知![]() 位于晶胞的顶点,数目为
位于晶胞的顶点,数目为![]() 个,
个,![]() 位于体心,有1个,
位于体心,有1个,![]() 位于面心,数目为
位于面心,数目为![]() 个,故化学式为
个,故化学式为![]() ,由晶胞结构可知
,由晶胞结构可知![]() ,所以
,所以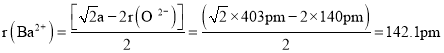 ;
;
故答案为:![]() ;
;![]() 。
。

 期末1卷素质教育评估卷系列答案
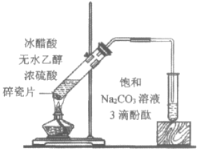
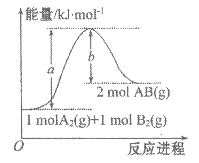
期末1卷素质教育评估卷系列答案【题目】下列实验所得结论正确的是
① | ② | ③ | ④ |
|
|
|
|
充分振荡试管,下层溶液红色褪去 | 溶液变红 | 溶液变红 | 充分振荡右侧小试管, 下层溶液红色褪去 |
A.①中溶液红色褪去的原因是:CH3COOC2H5+NaOH![]() CH3COONa+C2H5OH
CH3COONa+C2H5OH
B.②中溶液变红的原因是:CH3COO-+H2O![]() CH3COOH+H+
CH3COOH+H+
C.由实验①、②、③推测,①中红色褪去的原因是乙酸乙酯萃取了酚酞
D.④中红色褪去证明右侧小试管中收集到的乙酸乙酯中混有乙酸