题目内容
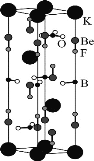
【题目】我国用BeO、KBF4等原料制备KBe2BO3F2晶体,在世界上首次实现在177.3 nm深紫外激光倍频输出,其晶胞如图所示。下列说法错误的是( )
A. 构成晶体的非金属元素的电负性由大到小的顺序为F>O>B
B. KBF4中的阴离子的中心原子的杂化方式为sp2
C. 根据元素周期表中元素所处的位置可推测BeO与Al2O3性质相似
D. 晶胞中的K+有2个位于晶胞内部,8个位于晶胞顶点,则1mo1该晶胞含3molKBe2BO3F2
【答案】B
【解析】
A.非金属元素的非金属性越强,电负性越大,则电负性由大到小的顺序为F>O>B,故A正确;
B. KBF4中的阴离子为BF4-,中心原子为B,根据价电子理论,中心原子价电子对数=4+![]() (4-4×1)=4,因此杂化方式为sp3,故B错误;
(4-4×1)=4,因此杂化方式为sp3,故B错误;
C. 根据对角线规则,在对角线的元素,性质具有相似性,故C正确;
D. 晶胞中的K+有2个位于晶胞内部,8个位于晶胞顶点,该晶胞中K+的数目=8×![]() +2=3,则1mo1该晶胞含3molK,因此KBe2BO3F2物质的量为3mol,故D正确;
+2=3,则1mo1该晶胞含3molK,因此KBe2BO3F2物质的量为3mol,故D正确;
答案选B。

练习册系列答案
相关题目
【题目】下表中评价合理的是
选项 | 化学反应及其离子方程式 | 评 价 |
A | NaHSO4溶液与Ba(OH)2溶液反应至 SO42-沉淀完全: 2H++SO42-+Ba2++2OH- = BaSO4↓ + 2H2O | 正 确 |
B | 向碳酸镁溶液中加入足量稀盐酸: CO32-+2H+=CO2↑+H2O | 错误,碳酸镁不应写成离子形式 |
C | 向沸水中滴加饱和的氯化铁溶液至液体变为红褐色: Fe3++3H2O = Fe(OH)3↓+3H+ | 正 确 |
D | NaOH溶液中通入少量CO2反应:OH-+CO2=HCO3- | 正 确 |