��Ŀ����
����Ŀ����������AlN����һ���ۺ������������մɲ��ϣ��ܻ���ˮ�⣬������ʴ��ijС��̽����ʵ�����Ʊ�AlN���ⶨ��Ʒ���ȣ����ʵ�����¡���ش�
���Ʊ�AlN
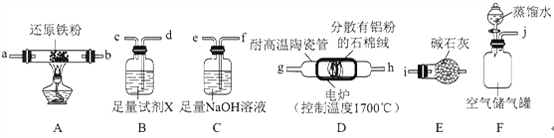
��1��ʵ��ʱ���Կ���Ϊԭ���Ʊ�AlN���������������ҵķ�������װ�õ���ȷ����˳��Ϊj��________��i���������ӿ���ĸ��ţ���
��2������װ���У���Ҫ��©����������Ϊ________��
��3���Լ�X������Ϊ________��
��4��װ��D�з�����Ӧ�Ļ�ѧ����ʽΪ________��
�ⶨ��Ʒ����
��5�����ʵ��֤����װ��D�IJ�Ʒ�к���Al����________��
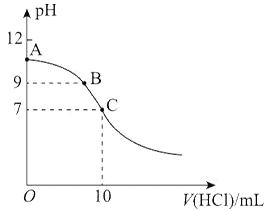
��6���ⶨ��Ʒ���ȣ�ȡװ��D�в�Ʒ4.37g����������NaOHŨ��Һ��ͨ��ˮ�����������ɵ�����ȫ����������V1mLc1mol��L��1���������գ��Է�̪��ָʾ������c2mol��L��1��NaOH����Һ�ζ����������ᣬ�ﵽ�ζ��յ�ʱ������V2mLNaOH����Һ����
�ٴﵽ�ζ��յ������Ϊ________��
�ڲ�Ʒ��A1N����������Ϊ________���г�����ʽ���ɣ���
���𰸡� f e d c a b����b a��g h����h g�� ��Һ©�� ���տ����е�ˮ�������������뻹ԭ���۷�Ӧ����ʵ�� 2Al��N2![]() 2AlN ȡD��������Ʒ���Թ��У���������ϡ���ᣬ����ɫ����ζ�Ŀ�ȼ���������ɣ����Ʒ�к���Al���� �������һ��NaOH����Һʱ����Һ����ɫǡ�ñ�Ϊdz��ɫ���Ұ���Ӳ���ɫ
2AlN ȡD��������Ʒ���Թ��У���������ϡ���ᣬ����ɫ����ζ�Ŀ�ȼ���������ɣ����Ʒ�к���Al���� �������һ��NaOH����Һʱ����Һ����ɫǡ�ñ�Ϊdz��ɫ���Ұ���Ӳ���ɫ ![]()
��������������������������۷�Ӧ�Ʊ�AlN ��ʵ��ʱ���Կ���Ϊԭ���Ʊ�����������ͨ������������Һ��������̼��ͨ��Ũ������ͨ����ԭ�����۳����������������۷�Ӧ���ɵ�������Ϊ��ֹ����������ˮ�⣬�Ʊ�װ�ú�С���ü�ʯ�ҽ��и����2����������װ����Ҫ��©����3���Լ�X��Ũ���ᣬ����Ϊ�����������4��װ��D�е��������۷�Ӧ���ɵ���������5��Al���������ᷴӦ�������������������ᷴӦ����������������6�������ɵ�����ȫ����������V1mLc1mol��L��1�Ĺ����������գ���Һ�����ԣ������̪��ָʾ������Һ����ɫ����c2mol��L��1��NaOH����Һ�ζ����������ᣬ�ﵽ�ζ��յ�ʱ�ʼ��ԣ���Һ�Էۺ�ɫ���ڵ�����������������Һ��Ӧ���ɰ�������Ӧ�ų��İ�����c2mol��L��1 V2mL��NaOH������V1mL c1mol��L��1�����ᣬ���ݹ�ϵʽ���㣻
�������������Ϸ�����1��ʵ��ʱ���������������ҵķ�������װ�õ���ȷ����˳��Ϊj��f e d c a b����b a��g h����h g����i����2������װ���У���Ҫ��©������Ϊ��Һ©������3���Լ�X��Ũ���ᣬ����Ϊ���տ����е�ˮ�������������뻹ԭ���۷�Ӧ����ʵ�飻��4��װ��D�з�Ӧ�Ļ�ѧ����ʽΪ2Al��N2![]() 2AlN����ȡD��������Ʒ���Թ��У���������ϡ���ᣬ����ɫ����ζ�Ŀ�ȼ�������������ɣ����Ʒ�к���Al���ʣ���6����ԭ��Һ�����ԣ����������Ƶĵ��룬��Һ��PH������Һ��Ϊ���ԣ����Ե������һ��NaOH����Һʱ����Һ����ɫǡ�ñ�Ϊdz��ɫ���Ұ���Ӳ���ɫ�ﵽ�ζ��յ㣻
2AlN����ȡD��������Ʒ���Թ��У���������ϡ���ᣬ����ɫ����ζ�Ŀ�ȼ�������������ɣ����Ʒ�к���Al���ʣ���6����ԭ��Һ�����ԣ����������Ƶĵ��룬��Һ��PH������Һ��Ϊ���ԣ����Ե������һ��NaOH����Һʱ����Һ����ɫǡ�ñ�Ϊdz��ɫ���Ұ���Ӳ���ɫ�ﵽ�ζ��յ㣻
�� �赪����������Ϊx g
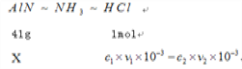
![]()
X=![]() ����Ʒ��A1N����������Ϊ
����Ʒ��A1N����������Ϊ![]()

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�