��Ŀ����
17����ͬ���ʵ�����Fe��Mg��Al��Na��0.1molͶ�뵽��HCl 0.01mol��ϡ�����У��û���H2�ɶൽ�ٵ�˳���ǣ�������| A�� | Al��Mg=Fe��Na | B�� | Al=Mg=Fe=Na | C�� | Na��Al��Mg��Fe | D�� | Al=Mg=Fe��Na |
���� ���ʱ���ƿ���ˮ��Ӧ������������Fe��Mg��Alֻ�������ᷴӦ����Na���ᷴӦʱ��Na����ȫ��Ӧ������2Na��H2���������������ʵ���������Fe+2HCl=FeCl2+H2����Mg+2HCl=MgCl2+H2����2Al+6HCl=2AlCl3+3H2�������й������㣬���ݲ����������ʼ���������������ͬ�����£����֮�ȵ������ʵ���֮�ȣ�
��� �⣺���ʱ���ƿ���ˮ��Ӧ������������Fe��Mg��Alֻ�������ᷴӦ����Na���ᷴӦʱ��Na����ȫ��Ӧ����2Na��H2����֪��0.1molNa��ȫ��Ӧ���������������ʵ���=0.1mol��$\frac{1}{2}$=0.05mol��
Fe+2HCl=FeCl2+H2��
0.1mol 0.2mol
������㣬�ɷ���ʽ��֪��������Ϊ0.005mol��
Mg+2HCl=MgCl2+H2��
0.1mol 0.2mol
������㣬�ɷ���ʽ��֪��������Ϊ0.005mol��
2Al+6HCl=2AlCl3+3H2��
0.1mol 0.3mol
������㣬�ɷ���ʽ��֪��������Ϊ0.005mol��
��ͬ�����£����֮�ȵ������ʵ���֮�ȣ������������������Al=Mg=Fe��Na��
��ѡD��
���� ���⿼���Ƶ����ʡ����ݷ���ʽ���㣬���й��������ǹؼ���ע���ƺ�ˮ��Ӧ���ص㣮

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | ��ˮ�ܵ��磬˵��NH3�ǵ���� | |
| B�� | ��ˮϡ�ͣ���Һ�е�c��OH-������ | |
| C�� | ����ϡ��������Һ��pH=7��c��NH4+��=c��SO42-�� | |
| D�� | ���з�̪�İ�ˮ�м�������NH4Cl���壬��Һ��ɫ��dz |
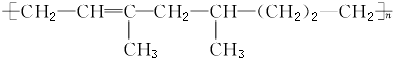
| A�� | �ø߾�����ͨ���Ӿ۷�Ӧ���ɵ� | |
| B�� | �ϳɸø߾���ĵ��������� | |
| C�� | 1 mol����������1 mol H2�ӳɣ����ɲ���̼̼˫�������� | |
| D�� | �ø߾����ܱ�����KMnO4��Һ���� |
| A�� | CH3COOH+CH3CH2OH$��_{����}^{Ũ����}$CH3COOCH2CH33+H2O | |
| B�� | 2CH3CH2OH+O2 $��_{��}^{����}$ 2CH3CHO+2H2O | |
| C�� | CH4+Cl2$\stackrel{��}{��}$CH3Cl+HCl | |
| D�� | 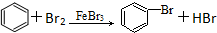 |
| A�� | 1mol/L | B�� | 1.5 mol/L | C�� | 2 mol/L | D�� | 3 mol/L |
| A�� | �����Ȼ�����Һʱ��Ӧʹ������е�ˮ����ȫ���ɺ���ֹͣ���� | |
| B�� | ����ʯ��ʱ��Ӧʹ�¶ȼ�ˮ�������Һ������ | |
| C�� | ��Һ����ʱ���²�Һ��ӷ�Һ©���¿ڷų����ϲ�Һ����Ͽڷŵ���һ���ձ� | |
| D�� | ������������ӵIJ������ȼ������ữ�ټ����Ȼ�����Һ |
| A�� | N2��H2��NH3�İٷֺ������ | |
| B�� | ��λʱ�䣬����a mol N2��ͬʱ����3mol H2 | |
| C�� | ��λʱ�䣬����a molN2��ͬʱ����3a mol H2 | |
| D�� | ��Ӧ���ڶ��ݵ������н��У��¶�һ��ʱ��ѹǿ����ʱ��ı� |
