题目内容
【题目】某直链有机化合物A分子中碳、氢元素的总质量分数为0.814,A的相对分子质量小于90,其余为氧元素质量分数。
(1)求该有机化合物A的分子式;
(2)A可以与金属钠作用放出氢气,能使溴的四氯化碳溶液褪色,写出该化合物A可能的三种结构简式。
【答案】(1)C5H10O;(2)CH2=CHCH2CH2CH2OH、CH3CH=CHCH2CH2OH、CH3CH2CH=CHCH2OH、CH2=C(CH3)CH2CH2OH、CH2= CHCH(CH3)CH2OH、CH2=CHC(CH3)2OH等(其他合理答案均可)
【解析】(1)化合物A氧元素的质量分数为1-0.814=0.186,A分子中O原子数目最多为![]() =1,故A分子中含有1个O原子,A的相对分子质量为
=1,故A分子中含有1个O原子,A的相对分子质量为![]() =86,剩余基团的式量为86-16=70,分子中碳原子最大数目为
=86,剩余基团的式量为86-16=70,分子中碳原子最大数目为![]() =5…10,故剩余基团为C5H10,故A的分子式为C5H10O,故答案为:C5H10O;
=5…10,故剩余基团为C5H10,故A的分子式为C5H10O,故答案为:C5H10O;
(2)不饱和度为![]() =1,A可以与金属钠作用放出氢气,能使溴的四氯化碳溶液褪色,则A含有1个C=C双键、1个-OH,故A的结构简式为CH2=CHCH2CH2CH2OH、CH3CH=CHCH2CH2OH、CH3CH2CH=CHCH2OH、CH2=C(CH3)CH2CH2OH、CH2= CHCH(CH3)CH2OH 、CH2=CHC(CH3)2CH2OH等,故答案为:CH2=CHCH2CH2CH2OH、CH3CH=CHCH2CH2OH、CH3CH2CH=CHCH2OH、CH2=C(CH3)CH2CH2OH、CH2= CHCH(CH3)CH2OH 、CH2=CHC(CH3)2OH等(其他合理答案均可)。
=1,A可以与金属钠作用放出氢气,能使溴的四氯化碳溶液褪色,则A含有1个C=C双键、1个-OH,故A的结构简式为CH2=CHCH2CH2CH2OH、CH3CH=CHCH2CH2OH、CH3CH2CH=CHCH2OH、CH2=C(CH3)CH2CH2OH、CH2= CHCH(CH3)CH2OH 、CH2=CHC(CH3)2CH2OH等,故答案为:CH2=CHCH2CH2CH2OH、CH3CH=CHCH2CH2OH、CH3CH2CH=CHCH2OH、CH2=C(CH3)CH2CH2OH、CH2= CHCH(CH3)CH2OH 、CH2=CHC(CH3)2OH等(其他合理答案均可)。

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案【题目】苯甲酸广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸。反应原理: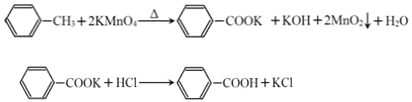
已知:甲苯的熔点为﹣95℃,沸点为110.6℃,易挥发,密度为0.866g/cm3;
苯甲酸的熔点为122.4℃,在25℃和95℃下在水中溶解度分别为0.344g和6.8g。
Ⅰ.【制备产品】将30.0mL甲苯和25.0mL 1mol/L高锰酸钾溶液在100℃下反应30min,装置如图1所示:
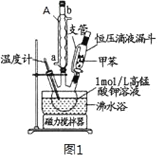
(1)仪器A的名称为________,A的进水口为___(填“a”或“b”)。支管的作用是____________。
(2)在本实验中,三颈烧瓶最合适的容积是____(填字母).
A.50mL B.100mL C.250mL D.500mL
Ⅱ.【分离产品】该同学设计如图2流程分离粗产品苯甲酸和回收甲苯。

(3)操作Ⅰ的名称是________;含有杂质的产物经操作Ⅱ进一步提纯得无色液体甲苯,则操作Ⅱ的名称是_________。
Ⅲ.【纯度测定】称取1.220g白色固体,配成100mL甲醇溶液,取25.00mL溶液,用0.1000mol/LKOH标准溶液滴定,重复滴定四次,每次消耗的体积如表所示.
第一次 | 第二次 | 第三次 | 第四次 | |
体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
(4)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果______(填“偏大”、“偏小”或“不变”).计算样品中苯甲酸纯度为_________。
(5)从白色固体B中得到纯净的苯甲酸的实验方法是:____________________。