题目内容
4.抗酸药物的种类很多,其有效成分一般都是碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝和氢氧化镁等化学物质.(1)抗酸药物具有抗酸作用的原因是其有效成分都能中和胃里过多的盐酸.
(2)某品牌抗酸药的主要成分有糖衣、碳酸镁、氢氧化铝、淀粉.
①写出该抗酸药发挥功效时的离子方程式:MgCO3+2H+═Mg2++CO2↑+H2O、Al(OH)3+3H+═Al3++3H2O.
②淀粉在抗酸药中作填充剂、粘合剂,淀粉在人体内酶的催化作用下发生水解反应,最终转化为(写分子式)C6H12O6.
分析 (1)根据抗酸药物有效成分能中和胃里过多的盐酸分析;
(2)①碳酸镁和盐酸反应生成氯化镁、水和二氧化碳,氢氧化铝和盐酸反应生成氯化铝和水,根据化学方程式改写离子方程式;
②根据淀粉在人体内在酶的作用水解最终转化成葡萄糖判断.
解答 解:(1)碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝和氢氧化镁都能中和胃里过多的盐酸,故答案为:其有效成分都能中和胃里过多的盐酸;
(2)①碳酸镁和盐酸反应生成氯化镁、水和二氧化碳,反应的离子方程式为:MgCO3+2H+═Mg2++CO2↑+H2O;氢氧化铝和盐酸反应生成氯化铝和水,反应的离子方程式为:Al(OH)3+3H+═Al3++3H2O,故答案为:MgCO3+2H+═Mg2++CO2↑+H2O;Al(OH)3+3H+═Al3++3H2O;
②淀粉在人体内在酶的作用水解最终转化成葡萄糖,其化学式为:C6H12O6,故答案为:C6H12O6.
点评 本题考查了酸碱盐之间的复分解反应及离子方程式的书写,难度不大,必须正确写出化学方程式才能正确解答.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.下列关于分子间作用力的说法,正确的是( )
| A. | 分子间作用力是一种比较弱的化学键 | |
| B. | 氯化钠晶体中不存在范德华力 | |
| C. | 锂、钠、钾、铷、铯的熔点越来越低是因为分子间作用力越来越弱 | |
| D. | 分子间作用力越大,分子的热稳定性就越大 |
15.下列各组物质中,符合前者为混合物,后者为单质的是( )
| A. | Na2CO3•10H2O Na2CO3 | B. | 冰水混合物 液氮 | ||
| C. | 石油 液氢 | D. | 碘酒 干冰 |
12.对室温下c(H+)相同、体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是( )
| A. | 加适量的醋酸钠晶体后,两溶液的c(H+)均减小 | |
| B. | 使温度都升高20℃后,两溶液的c(H+)均不变 | |
| C. | 加水稀释2倍后,两溶液的c(H+)均增大 | |
| D. | 加足量的锌充分反应后,两溶液中产生的氢气一样多 |
19.分子式为C9H18O2的有机物A,在硫酸存在下与水反应生成B、C两种物质,C经一系列氧化最终可转化为B的同类物质,又知等质量的B、C的蒸气在同温同压下所占体积相同,则A的酯类同分异构体共有( )
| A. | 8种 | B. | 12种 | C. | 16种 | D. | 18种 |
9.将质量相等的下列各物质完全酯化时,需醋酸质量最多的是( )
| A. | 甲醇 | B. | 乙二醇 | C. | 丙醇 | D. | 甘油 |
16.对于反应A(g)+3B(g)═2C(g),下列各数据表示不同条件下的反应速率,其中反应进行的最快的是( )
| A. | v(A)=0.01mol•L-1•s-1 | B. | v(B)=0.02mol•L-1•s-1 | ||
| C. | v(B)=1.7mol•L-1•min-1 | D. | v(C)=1.0mol•L-1•min-1 |
13.下列关于晶体的说法一定正确的是( )
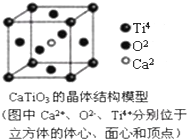

| A. | 分子晶体中都存在共价键 | |
| B. | CaTiO3晶体中每个Ti4+和12个O2-相紧邻 | |
| C. | SiO2晶体中每个硅原子与两个氧原子以共价键相结合 | |
| D. | 金属晶体的熔点都比分子晶体的熔点高 |
14.溶液中粒子的物质的量浓度关系一定正确的是( )
| A. | 0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液:c(Na+)>c(CO32-)>c(HCO3- )>c(OH-) | |
| B. | pH相等的①NH4Cl ②(NH4)2SO4 ③NH4HSO4溶液中,c(NH4+)大小顺序:①=②>③ | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(H+)>c(NH4+ )>c(OH-) | |
| D. | 0.2mol•L-1CH3COOH溶液与0.1mol•L-1NaOH溶液等体积混合:2c(H+)-2c(OH-)═C(CH3COO-)+C(CH3COOH) |