题目内容
19.将质量分数为x的氨水与水等质量混合,质量分数为a,若与水等体积混合,质量分数为b,将质量分数为x的NaOH溶液与水等体积混合,质量分数为c,则a、b、c大小关系为( )| A. | a>b>c | B. | c>a>b | C. | b>c>a | D. | b>a>c |
分析 假设氨水与水的质量均为m,混合后溶液质量为2m,根据质量分数计氨水中氨气的质量,混合恰好氨气的质量不变,可以计算混合溶液质量分数;
水的密度为1g/mol,设溶液的密度为dg/mL,水与溶液的体积均为VL,计算溶质的质量及混合后溶液总质量,表示出混合后的质量分数,结合氨水的密度<1g/mL、氢氧化钠溶液的密度>1g/mL分析判断.
解答 解:假设氨水与水的质量均为m,混合后溶液质量为2m,氨气的质量为mx,则混合后质量分数a=$\frac{mx}{2m}$=0.5x;
水的密度为1g/mol,设溶液的密度为dg/mL,水与溶液的体积均为VmL,则溶质的质量为Vdx g,则混合后溶液质量分数=$\frac{Vdx}{V+Vd}$=$\frac{dx}{1+d}$=$\frac{d}{1+d}$x,
氨水的密度<1g/mL,则$\frac{d}{1+d}$<$\frac{1}{2}$,即b=$\frac{d}{1+d}$x<0.5x,
氢氧化钠溶液的密度>1g/mL,则$\frac{d}{1+d}$>$\frac{1}{2}$,即c=$\frac{d}{1+d}$x>0.5x,
故c>a>b,
故选:B.
点评 本题考查了有关溶质质量分数的计算,难度不大,注意对规律的归纳总结:①等质量混合,混合后溶液质量分数等于两种溶液中溶质的质量分数之和的一半;②密度比水大的两种不同浓度溶液混合,等体积混合后所得溶液中溶质的质量分数大于两种溶液中溶质的质量分数之和的一半,③密度比水小的两种不同浓度溶液混合,等体积混合后所得溶液中溶质的质量分数小于两种溶液中溶质的质量分数之和的一半.

练习册系列答案
相关题目
10. 神舟七号返回舱约3吨多重,是世界上现有的最大的返回舱.为了防止飞船与大气摩擦产生高温而起火燃烧,在飞船表面覆盖着某种特殊材料,该材料应具有的性质是( )
神舟七号返回舱约3吨多重,是世界上现有的最大的返回舱.为了防止飞船与大气摩擦产生高温而起火燃烧,在飞船表面覆盖着某种特殊材料,该材料应具有的性质是( )
 神舟七号返回舱约3吨多重,是世界上现有的最大的返回舱.为了防止飞船与大气摩擦产生高温而起火燃烧,在飞船表面覆盖着某种特殊材料,该材料应具有的性质是( )
神舟七号返回舱约3吨多重,是世界上现有的最大的返回舱.为了防止飞船与大气摩擦产生高温而起火燃烧,在飞船表面覆盖着某种特殊材料,该材料应具有的性质是( )| A. | 良好的导电性 | |
| B. | 密度较大,以增大飞船对地面的惯性 | |
| C. | 轻质防热,可以承受上千度的高温 | |
| D. | 质地柔软,以利于飞船变形 |
4.在配制一定物质的量浓度的溶液时,不会用到的仪器是( )
| A. |  烧杯 | B. |  烧瓶 | C. |  容量瓶 | D. |  胶头滴管 |
8.铺设铁路的钢轨所用的合金钢中含有( )
| A. | 钨 | B. | 硅 | C. | 锰 | D. | 铬和镍 |
9.若以w1和w2分别表示物质的量浓度为a mol/L和b mol/L氨水的溶质质量分数,且w2=2w1,则下列判断正确的是( )
| A. | 2a=b | B. | a=2b | C. | 2a<b | D. | a<b<2a |
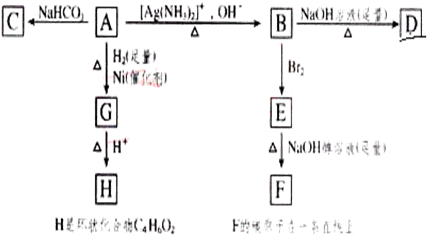
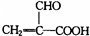 .
.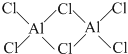 在X、Y、Z、W四种元素中,X是原子半径最小的元素;Y的基态原子中电子占据了三种能量不同的原子轨道,且这三种轨道中的电子数相同;Z的原子最外层电子数是内层的3倍;W基态原子的3p原子轨道上有4个电子.
在X、Y、Z、W四种元素中,X是原子半径最小的元素;Y的基态原子中电子占据了三种能量不同的原子轨道,且这三种轨道中的电子数相同;Z的原子最外层电子数是内层的3倍;W基态原子的3p原子轨道上有4个电子.