题目内容
【题目】通过海水晾晒可得粗盐。粗盐除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质。某同学用某种粗盐进行提纯实验,步骤见下图。请回答下列问题:
![]()
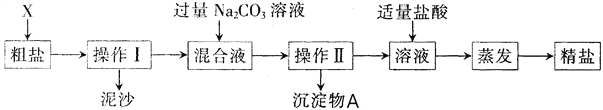
(1)在完成操作Ⅰ之前,必须加入的X物质是___________________。
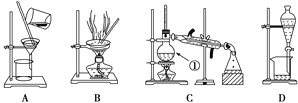
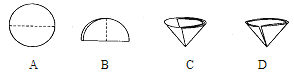
(2)操作Ⅰ和操作Ⅱ的名称是__________________________。该操作中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是___________________________(填序号)。
(3)在蒸发操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外还可采取_____________________________________________________等措施。
(4)判断加入的盐酸“适量”的方法是_______________________________________________________________________________。
(5)实验所得精盐的质量___________________________(填“大于”、“小于”或“等于”)粗盐中NaCl的质量,原因是_________________________________________________________________________________。
(6)猜想和验证:(并完成相应填空)
猜想 | 验证的方法 | 现象 | 结论 |
猜想Ⅰ:沉淀物A中含CaCO3、MgCO3 | 取少量沉淀物A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 | __________ | 猜想Ⅰ成立 |
猜想Ⅱ:沉淀物A中含BaCO3 | 取少量沉淀物A于试管中,先滴入________,再滴入Na2SO4溶液 | 有气泡放出,无白色沉淀 | ______ |
猜想Ⅲ:最后制得的NaCl晶体中还含有Na2SO4 | 取少量NaCl晶体溶于试管中的蒸馏水,____________________ | __________ | 猜想Ⅲ成立 |
【答案】 水 过滤 D 间歇加热(或“来回移动酒精灯或蒸发皿”) 滴加盐酸至无气泡放出为止或测定pH 大于 提纯的过程中有氯化钠生成 有气泡放出 烧杯底变浑浊(或石灰水变浑浊,或石灰水有白色沉淀) 滴入稀硝酸(或稀盐酸) 猜想Ⅱ不成立 滴入BaCl2[或Ba(OH)2、或Ba(NO)3]溶液,有白色沉淀
【解析】(1)在完成操作Ⅰ之前,必须用水溶解粗盐。故必须加入的X物质是:水;(2)操作Ⅰ和操作Ⅱ的名称是过滤,通过过滤可以把不溶于水的物质除去;如图2中不该出现的情形是D,因为D出现了裂缝;(3)玻璃棒不断搅拌,来回移动酒精灯加热,或间歇加热,都可以使液体均匀受热,能够防止液体外溅;(4)判断加入的盐酸“适量”的方法是滴加盐酸至无气泡放出为止或测定pH;(5)因为除氯化镁和氯化钙杂质、除过量的氢氧化钠和碳酸钠的过程中都生成了氯化钠,所以实验所得精盐的质量大于粗盐中NaCl的质量;(3)假设猜想1成立:则有气泡放出,烧杯底变浑浊(或石灰水变浑浊,或石灰水有白色沉淀);猜想Ⅱ取少量沉淀物A于试管中,先滴入稀硝酸(或稀盐酸),再滴入Na2SO4溶液无沉淀产生,说明溶液中不含钡离子,猜想II不成立;猜想Ⅲ取少量NaCl晶体溶于试管中的蒸馏水,滴入BaCl2[或Ba(OH)2、或Ba(NO)3]溶液,有白色沉淀产生,证明晶体中含有硫酸钠,猜想Ⅲ成立。

【题目】下列物质的分类正确的是( )
选项 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
A | Na2CO3 | H2SO4 | NaOH | SO2 | CO2 |
B | NaOH | HCl | NaCl | Na2O | NO |
C | KOH | HNO3 | CaCO3 | CaO | Mn2O7 |
D | NaOH | HCl | CaF2 | Na2O2 | SO2 |
A. A B. B C. C D. D