题目内容
【题目】下图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池)。下列有关说法不正确的是

A. 放电时正极反应为:NiOOH+H2O+e-===Ni(OH)2+OH-
B. 充电时负极反应为:MH+OH-===H2O+M+e-
C. 电池的电解液可为KOH溶液
D. MH是一类储氢材料,其氢密度越大,电池的能量密度越高
【答案】B
【解析】放电时,正极发生还原反应,其反应为:NiOOH+H2O+e-===Ni(OH)2+OH-,A正确;充电时负极发生还原反应,其反应为H2O+M+e-= MH+OH-,B错误;根据电池充放电的电极反应可知,电池的电解液为碱性溶液,所以可用KOH溶液,C正确;MH是一类储氢材料,其氢密度越大,电池的能量密度越高,D正确;正确选项B。

【题目】氯化铜晶体(CuCl2·2H2O)含有FeCl2杂质,为制得纯净氯化铜晶体,首先将其制成水溶液,然后按下列操作步骤进行提纯:

①先加入氧化剂X,再加入物质Y,过滤得沉淀Z。
②将滤液蒸发结晶得纯CuCl2·2H2O晶体。
已知:三种离子在溶液中完全变成氢氧化物沉淀所需pH值如下表。
离子 | Fe3+ | Cu2+ | Fe2+ |
pH | 3.7 | 6.4 | 6.4 |
试回答下列问题:
(1)加入氧化剂X的目的是______________________________________。
(2)下列物质都可以作为氧化剂,其中最适宜于本实验的是_________。
A.H2O2 B.KMnO4 C.NaClO D.K2Cr2O7
此过程发生反应的离子方程式为_____________________________________。
(3)物质Y可以用______________(填一种物质),沉淀Z是____________。
(4)为分离出沉淀Z采取的实验操作是_________________。
(5)步骤②所用的仪器有铁架台(含铁圈)、酒精灯、玻璃棒和_________,如要获得无水CuCl2,应采取的操作是____________________________________________。
【题目】下列装置所示的实验中,不能达到实验目的是
|
|
|
|
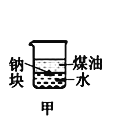
A.长时间看到Fe(OH)2白色沉淀 | B.证明ρ(煤油)< ρ(钠) < ρ(水) | C.探究氧化性: KMnO4>Cl2>I2 | D.比较NaHCO3、Na2CO3的热稳定性 |
A. A B. B C. C D. D