题目内容
【题目】已知2SO2(g)+O2(g)![]() 2SO3(g) △H=-197kJ/mol。在25℃时,向恒容密闭容器中通入2 mol SO2和1 mol O2,达到平衡时放出热量Q1;若25℃时在此恒容密闭容器中只通入1 mol SO2和0.5 mol O2,达到平衡时放出热量Q2。则下列关系正确的是
2SO3(g) △H=-197kJ/mol。在25℃时,向恒容密闭容器中通入2 mol SO2和1 mol O2,达到平衡时放出热量Q1;若25℃时在此恒容密闭容器中只通入1 mol SO2和0.5 mol O2,达到平衡时放出热量Q2。则下列关系正确的是
A. Q2>Q1>197 kJ B. 2Q2<Q1<197 kJ
C. 2Q2=Q1=197 kJ D. 197 kJ> Q1=2Q2
【答案】B
【解析】
2SO2(g)+O2(g)![]() 2SO3(g) △H=-197kJ/mol,表示在上述条件下2mol SO2和1molO2完全反应生成2molSO3气体放出热量为197kJ,再结合可逆反应中反应物不能完全反应解答。
2SO3(g) △H=-197kJ/mol,表示在上述条件下2mol SO2和1molO2完全反应生成2molSO3气体放出热量为197kJ,再结合可逆反应中反应物不能完全反应解答。
反应的热化学方程式为:2SO2(g)+O2(g)![]() 2SO3(g) △H=-197kJ/mol,由热化学方程式可知,在上述条件下反应生成2molSO3气体放热197kJ,加入2mol SO2和1molO2,生成SO3的物质的量小于2mol,所以Q1<197kJ,通入1mol SO2和0.5molO2,如果转化率与加入2mol SO2和1molO2相同,则放热为Q1/2kJ,但此时体系压强比加入2mol SO2和1molO2要小,所以平衡会向左移动,则实际放出的热量小于Q1/2kJ,即2Q2<Q1,综上得:2Q2<Q1<197kJ,答案选B。
2SO3(g) △H=-197kJ/mol,由热化学方程式可知,在上述条件下反应生成2molSO3气体放热197kJ,加入2mol SO2和1molO2,生成SO3的物质的量小于2mol,所以Q1<197kJ,通入1mol SO2和0.5molO2,如果转化率与加入2mol SO2和1molO2相同,则放热为Q1/2kJ,但此时体系压强比加入2mol SO2和1molO2要小,所以平衡会向左移动,则实际放出的热量小于Q1/2kJ,即2Q2<Q1,综上得:2Q2<Q1<197kJ,答案选B。

【题目】以废旧锌锰电池中的黑锰粉(MnO2、MnO(OH)、NH4Cl、少量ZnCl2及炭黑、氧化铁等)为原料制备MnCl2,实现锰的再利用。其工作流程如下:
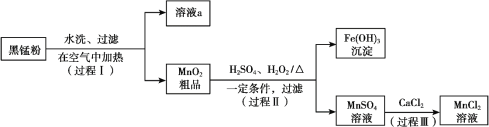
(1)过程Ⅰ,在空气中加热黑锰粉的目的是除炭、氧化MnO(OH)等。O2氧化MnO(OH)的化学方程式是_______。
(2)溶液a的主要成分为NH4Cl,另外还含有少量ZnCl2等。
① 溶液a呈酸性,原因是______。
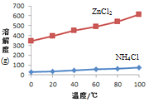
② 根据如图所示的溶解度曲线,将溶液a______(填操作),可得NH4Cl粗品。
③ 提纯NH4Cl粗品,有关性质数据如下:
化合物 | ZnCl2 | NH4Cl |
熔点 | 365℃ | 337.8℃分解 |
沸点 | 732℃ | ------------- |
根据上表,设计方案提纯NH4Cl:________。
(3)检验MnSO4溶液中是否含有Fe3+:取少量溶液,加入_______(填试剂和现象),证明溶液中Fe3+沉淀完全。
(4)探究过程Ⅱ中MnO2溶解的适宜条件。
ⅰ.向MnO2中加入H2O2溶液,产生大量气泡;再加入稀H2SO4,固体未明显溶解。
ⅱ.向MnO2中加入稀H2SO4,固体未溶解;再加入H2O2溶液,产生大量气泡,固体完全溶解。
① 用化学方程式表示ⅱ中MnO2溶解的原因:________。
② 解释试剂加入顺序不同,MnO2作用不同的原因:________。
上述实验说明,试剂加入顺序不同,物质体现的性质可能不同,产物也可能不同。