题目内容
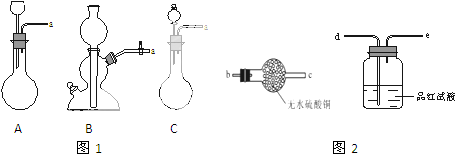
11.在化学课上,围绕浓硫酸的化学性质进行了如下实验探究:将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀.然后加入适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体.请回答:(1)生成的黑色(单质)物质是(填化学式)C.
(2)这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的主要污染物之一,这种刺激性气味的气体成分是(填化学式)SO2.
(3)据蔗糖与浓硫酸反应的实验现象,说明浓硫酸具有(填序号)CD.
A.酸性 B.吸水性 C.脱水性 D.强氧化性
(4)将实验(2)产生的刺激性气味气体通入品红溶液,可以看到品红溶液褪色,这说明这种气体具有漂白性;将(2)中产生的刺激性气味的气体通入水中可生成一中不稳定、易分解的酸,请写出该反应的化学方程式SO2+H2O?H2SO3.
分析 (1)将适量的蔗糖放入烧杯中,加几滴水,搅拌均匀,然后加入浓硫酸,生成黑色物质为碳;
(2)脱水过程中反应放热,所生产的碳和浓硫酸反应生成二氧化硫、二氧化碳和水;
(3)反应过程中表现了浓硫酸的脱水性生成碳,强氧化性和碳反应生成人欲横流和二氧化碳、水;
(4)产生的有刺激性气味的气体为二氧化硫,通入品红溶液中褪色,是二氧化硫的漂白性;二氧化硫与水反应生成亚硫酸;
解答 解:(1)将适量的蔗糖放入烧杯中,加几滴水,搅拌均匀,然后加入浓硫酸,把蔗糖中的氢元素和氧元素按照2:1脱去,生成黑色物质是C,体现了浓硫酸的脱水性,
故答案为:C;
(2)黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的主要污染物之一,这种刺激性气味的气体成分是二氧化硫,反应的化学方程式为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2H2O+2SO2↑,
故答案为:SO2;
(3)将适量的蔗糖放入烧杯中,加几滴水,搅拌均匀,然后加入浓硫酸,生成黑色物质碳表现了浓硫酸的脱水性,黑色物质继续与浓硫酸作用会产生两种气体,体现了浓硫酸的强氧化性,过程中为表现酸性和吸水性,
故答案为:CD;
(4)有刺激性气味的气体通入品红溶液中,可以看到品红溶液褪色,表现了二氧化硫的漂白性,二氧化硫和水反应生成亚硫酸,反应的化学方程式为:SO2+H2O?H2SO3,
故答案为:褪色;漂白;SO2+H2O?H2SO3.
点评 本题以浓硫酸和蔗糖的反应为载体考查浓硫酸的性质,题目难度中等,浓硫酸具有吸水性、脱水性和强氧化性,注意吸水性和脱水性的区别,明确二氧化硫能使氯水褪色是体现还原性而不是漂白性,为易错点.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
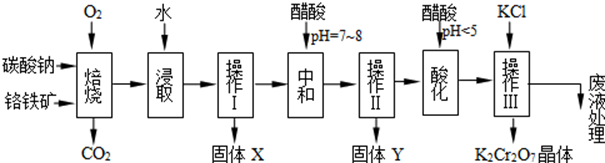
16.铬铁矿是主要成分可表示为FeO•Cr2O3,还含有还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的工艺流程.
已知1:
①4FeO•Cr2O3+8Na2CO3+7O2 $\stackrel{750℃}{→}$8Na2CrO4+2Fe2O3+8CO2↑;
②Na2CO3+Al2O3 $\stackrel{750℃}{→}$2NaAlO2+CO2↑;
③Cr2O72-+H2O?2CrO42-+2H+
根据题意回答下列问题:
(1)操作I的名称是过滤.
(2)下表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr207+2KCl=K2Cr207↓+2NaCl,该反应在溶液中能发生的理由是Na2Cr207的溶解度比K2Cr207大
(3)操作Ⅲ有多步组成,获得K2Cr207晶体的操作依次是:加入KC1固体、蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(4)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是:称取n g样品,加入过量NaOH溶液 (写试剂)、溶解、过滤、再通入足量CO2气体…灼烧、冷却、称量,得干燥固体m g.计算样品中氢氧化铝的质量分数为$\frac{26n}{17m}$ (用含m、n的代数式表示).
(5)称取重铬酸钾试样2.500g配成250mL溶液,取出25mL与碘量瓶中,加入10mL 2mol/L H2SO4和足量碘化钾,放于暗处5min.然后加入100mL水,加入3mL 淀粉指示剂,用0.1000mol/LNa2S203标准溶液滴定,若实验中共用去Na2S203标准溶液47.40mL,则所得产品中重铬酸钾的纯度为92.9%.(保留3位有效数字)
已知:
①K2Cr2O7的摩尔质量为294g/mol
②Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O;
I2+2S2O32-=2I-+S4O62-.

已知1:
①4FeO•Cr2O3+8Na2CO3+7O2 $\stackrel{750℃}{→}$8Na2CrO4+2Fe2O3+8CO2↑;
②Na2CO3+Al2O3 $\stackrel{750℃}{→}$2NaAlO2+CO2↑;
③Cr2O72-+H2O?2CrO42-+2H+
根据题意回答下列问题:
(1)操作I的名称是过滤.
(2)下表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr207+2KCl=K2Cr207↓+2NaCl,该反应在溶液中能发生的理由是Na2Cr207的溶解度比K2Cr207大
| 物质 | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
| 溶解度(g/100g水) | 0℃ | 28 | 35.7 | 4.7 | 163 |
| 40℃ | 40.1 | 36.4 | 26.3 | 215 | |
| 80℃ | 51.3 | 38 | 73 | 376 | |
(4)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是:称取n g样品,加入过量NaOH溶液 (写试剂)、溶解、过滤、再通入足量CO2气体…灼烧、冷却、称量,得干燥固体m g.计算样品中氢氧化铝的质量分数为$\frac{26n}{17m}$ (用含m、n的代数式表示).
(5)称取重铬酸钾试样2.500g配成250mL溶液,取出25mL与碘量瓶中,加入10mL 2mol/L H2SO4和足量碘化钾,放于暗处5min.然后加入100mL水,加入3mL 淀粉指示剂,用0.1000mol/LNa2S203标准溶液滴定,若实验中共用去Na2S203标准溶液47.40mL,则所得产品中重铬酸钾的纯度为92.9%.(保留3位有效数字)
已知:
①K2Cr2O7的摩尔质量为294g/mol
②Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O;
I2+2S2O32-=2I-+S4O62-.
3.已知:常温下,0.01mol•L-1MOH溶液的pH为10,MOH(aq)与H2SO4(aq)反应生成1mol正盐的△H=-24.2kJ•mol-1,强酸与强酸稀溶液反应的中和热为△H=-57.3kJ•mol-1,则MOH的水溶液中电离的△H为( )
| A. | -69.4kJ•mol-1 | B. | -45.2kJ•mol-1 | C. | +69.4kJ•mol-1 | D. | +45.2kJ•mol-1 |
20.生活中处处有化学,下列表述不正确的是( )
| A. | 玻璃、陶瓷、水泥、光导纤维的化学组成都是硅酸盐 | |
| B. | 污水处理中的化学方法有混凝法、中和法、沉淀法、氧化还原法等 | |
| C. | 对不可回收垃圾常用的处理方法有卫生填埋、堆肥和焚烧 | |
| D. | 固体煤经处理变为气体燃料后,可以减少SO2和烟尘的污染,且燃烧效率高 |
1.下列有关(NH4)2Fe(SO4)2溶液的叙述正确的是( )
| A. | 该溶液中,Na+、H+、Cl-、NO3-可以大量共存 | |
| B. | 和新制氯水反应的离子方程式:Fe2++Cl2=Fe3++2Cl- | |
| C. | 加入NaOH溶液至Fe2+刚好沉淀完全的离子方程式:Fe2++2OH-=Fe(OH)2↓ | |
| D. | 离子浓度关系:c(SO42-)=c(NH4+ )>c(Fe2+ )>c(H+ )>c(OH-) |