题目内容
3.下列溶液中的c(Cl-)与50mL 1mol/L FeCl3溶液中的c(Cl-)相等的是( )| A. | 150mL 1mol/L NaCl溶液 | B. | 75mL 2mol/L NH4Cl溶液 | ||
| C. | 150mL 1.5mol/L MgCl2溶液 | D. | 75mL 2mol/L AlCl3溶液 |
分析 50mL1mol/L的feCl3溶液中的Cl-浓度为3mol/L,根据溶质化学式计算各选项中的Cl-物质的量,进行比较可知.注意溶液中溶质离子的浓度与溶液体积无关,只取决于物质电离出的离子的数目多少与溶质的浓度.
解答 解:50mL1mol/L的AlCl3溶液中的Cl-浓度为3mol/L,
A.150ml1mol/L的NaCl溶液中Cl-浓度为1mol/L,与50mL1mol/L的FeCl3溶液中的Cl-浓度不相等,故A错误;
B.75mL 2mol/L NH4Cl溶液中Cl-浓度为2mol/L,与50mL1mol/L的FeCl3溶液中的Cl-浓度不相等,故B错误;
C.150ml 1.5mol/L的MgCl2溶液中Cl-浓度为3mol/L,与50mL1mol/L的FeCl3溶液中的Cl-浓度相等,故C正确;
D.75ml 2mol/L AlCl3溶液中Cl-浓度为6mol/L,与50mL1mol/L的FeCl3溶液中的Cl-浓度不相等,故D错误;
故选C.
点评 本题考查物质的量浓度的计算与判断,题目难度不大,注意溶液中溶质离子的浓度与溶液体积无关,只取决于物质电离出的离子的数目多少与溶质的浓度.

练习册系列答案
相关题目
14.下列有关溶液物质的量浓度的说法正确的是( )
| A. | 把1 molNaCl溶于1 L水中所得溶液物质的量浓度为1mol/L | |
| B. | 把0.1molNaCl投入100mL容量瓶中加水至刻度线,充分振荡后浓度为1 mol/L | |
| C. | 把7.4gCa(OH)2放入烧杯中,加水搅拌冷却后全部转移到100 mL容量瓶并加水至刻度线,浓度为1 mol/L | |
| D. | 需要78 mL 0.1 mol/L的Na2CO3溶液,应选用l00 mL容量瓶 |
11.“纳米材料”是粒子直径为1~100nm(纳米)的材料,纳米碳就是其中的一种.若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸
⑤不能透过滤纸 ⑥静置后,会析出黑色沉淀 ⑦能透过半透膜.
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸
⑤不能透过滤纸 ⑥静置后,会析出黑色沉淀 ⑦能透过半透膜.
| A. | ①④⑥⑦ | B. | ②③④ | C. | ②③⑤⑦ | D. | ①③④⑥ |
18.在乙醇CH3CH2OH中化学键如图,则下列说法中正确的是( )
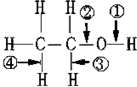

| A. | 当该醇发生催化氧化时,被破坏的键是②③ | |
| B. | 当该醇与Na反应时,被破坏的键是① | |
| C. | 当该醇与羧酸发生酯化反应时,被破坏的键是② | |
| D. | 当该醇发生消去反应时,被破坏的键是①和④ |
8.某一元醇7.4克完全与乙酸反应,可生成乙酸某酯11.6克.则其分相对分子质量为( )
| A. | 32 | B. | 60 | C. | 74 | D. | 88 |
15.NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | Na2O2与水反应制O2,每生成0.25molO2转移电子数为1NA | |
| B. | 等物质的量的N2和CO所含原子数均为2NA | |
| C. | 在标准状况下,11.2L HCHO所含的分子数约为0.5NA | |
| D. | 1molSO2与足量的O2反应,转移的电子数为2NA |
 ;
;