题目内容
【题目】常温下,向10mL0.1mol·L-1KCl溶液和10mL0.1mol·L-1K2CrO4溶液中分别滴加0.1mol·L-1AgNO3溶液。滴加过程中pM[表示-lgc(Cl-)或-lgc(CrO42-)]与所加AgNO3溶液体积之间的关系如下图所示。已知Ag2CrO4为砖红色沉淀,下列说法不合理的是
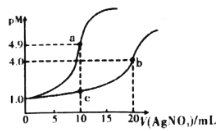
A.bc所在曲线对应K2CrO4溶液
B.常温下,Ksp(Ag2CrO4)<Ksp(AgCl)
C.溶液中c(Ag+)的大小:a点>b点
D.用0.1mol·L-1AgNO3标准液滴定上述KCl、K2CrO4溶液时,Cl-先沉淀
【答案】C
【解析】
由反应Cl-+Ag+=AgCl↓和CrO42-+2Ag+=Ag2CrO4↓分析,10mL0.1molL-1KCl溶液和10mL 0.1molL-1K2CrO4溶液中分别滴加等浓度的AgNO3溶液,当加入AgNO310mL时Cl-恰好完全沉淀,当加入AgNO3 20mL时,CrO42-沉淀完全,据此分析反应对应曲线。
A.常温下,向10mL0.1molL-1KCl溶液和10mL0.1molL-1K2CrO4溶液中分别滴加0.1molL-1AgNO3溶液,当加入10mLAgNO3溶液时,KCl恰好完全反应,加入20mLAgNO3溶液时K2CrO4恰好完全反应,因此a点所在曲线表示KCl溶液中变化的曲线,b、c点所在曲线表示K2CrO4溶液中的变化曲线,故A正确;
B.a点时恰好反应生成AgCl,由题图可知,此时-lgc(Cl-)=4.9,则溶液中c(Cl-)=1×10-4.9molL-1,c(Ag+)=![]() ,该温度下,Ksp(AgCl)=c(Cl-)×c(Ag+)=1×10-9.8,b点时恰好反应生成Ag2(CrO4),由题图可知,此时-lgc(CrO42-)=4.0,则溶液中c(CrO42-)=1×10-4 molL-1,c(Ag+)=2×10-4 molL-1,该温度下,Ksp(Ag2CrO4)=c(CrO42-)×c2(Ag+)=4×10-12,Ksp(Ag2CrO4)<Ksp(AgCl),故B正确;
,该温度下,Ksp(AgCl)=c(Cl-)×c(Ag+)=1×10-9.8,b点时恰好反应生成Ag2(CrO4),由题图可知,此时-lgc(CrO42-)=4.0,则溶液中c(CrO42-)=1×10-4 molL-1,c(Ag+)=2×10-4 molL-1,该温度下,Ksp(Ag2CrO4)=c(CrO42-)×c2(Ag+)=4×10-12,Ksp(Ag2CrO4)<Ksp(AgCl),故B正确;
C.溶液中a点c(Ag+)=1×10-4.9molL-1,b点c(Ag+)=2×10-4 molL-1,则a点<b点,故C错误;
D.用0.1mol·L-1AgNO3标准液滴定上述KCl、K2CrO4溶液时,对于KCl溶液c(Ag+)= ![]() =
= ![]() =1×10-8.8 molL-1,对于K2CrO4溶液c(Ag+)=
=1×10-8.8 molL-1,对于K2CrO4溶液c(Ag+)=![]() =
= ![]() =6.33×10-6 molL-1,则Cl-沉淀所需Ag+浓度小,Cl-先沉淀,故D正确;
=6.33×10-6 molL-1,则Cl-沉淀所需Ag+浓度小,Cl-先沉淀,故D正确;
答案为C。

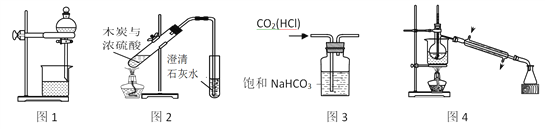
【题目】用如图装置进行实验,将液体a逐滴加到固体b中,下列叙述正确的是
选项 | a | b | c | 现象 | 装置图 |
A | 浓H2SO4 | Cu | 澄清石灰水 | c中溶液变浑浊 |
|
B | 浓盐酸 | KMnO4晶体 | 紫色石蕊溶液 | c中溶液最终呈红色 | |
C | 稀HNO3 | Fe | NaOH溶液 | d中红棕色气体变浅 | |
D | 浓氨水 | 生石灰 | Al2(SO4)3溶液 | c中产生沉淀后溶解 |
A.AB.BC.CD.D