题目内容
某工厂的废金属屑的主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,该厂用上述废金属屑制取新型高效水处理剂Na2FeO4(高铁酸钠)等产品,过程如下:
Ⅰ.向废金属屑中加入过量的NaOH溶液,充分反应后过滤;
Ⅱ.向Ⅰ所得固体中加入过量稀H2SO4,充分反应后过滤;
Ⅲ.向Ⅱ所得固体中继续加入热的稀H2SO4,同时不断鼓入空气,固体溶解得CuSO4溶液;
Ⅳ.……
(1)步骤Ⅰ中发生反应的化学方程式为___________、______________。
(2)步骤Ⅱ所得的滤液中加入KSCN溶液无明显现象,表明滤液中不存在Fe3+,用离子方程式解释其可能的原因:__________。
(3)步骤Ⅲ获得CuSO4溶液的离子方程式为____________。
(4)步骤Ⅱ所得滤液经进一步处理可制得Na2FeO4,流程如下:
ⅰ.H2O2ⅱ.调pHNaClO/NaOH混合溶液
①测得滤液中c(Fe2+)为a mol·L-1,若要处理1 m3滤液,理论上需要消耗25%的H2O2溶液________kg(用含a的代数式表示)。
②写出由Fe(OH)3制取Na2FeO4的化学方程式:_____________。
Ⅰ.向废金属屑中加入过量的NaOH溶液,充分反应后过滤;
Ⅱ.向Ⅰ所得固体中加入过量稀H2SO4,充分反应后过滤;
Ⅲ.向Ⅱ所得固体中继续加入热的稀H2SO4,同时不断鼓入空气,固体溶解得CuSO4溶液;
Ⅳ.……
(1)步骤Ⅰ中发生反应的化学方程式为___________、______________。
(2)步骤Ⅱ所得的滤液中加入KSCN溶液无明显现象,表明滤液中不存在Fe3+,用离子方程式解释其可能的原因:__________。
(3)步骤Ⅲ获得CuSO4溶液的离子方程式为____________。
(4)步骤Ⅱ所得滤液经进一步处理可制得Na2FeO4,流程如下:
ⅰ.H2O2ⅱ.调pHNaClO/NaOH混合溶液
①测得滤液中c(Fe2+)为a mol·L-1,若要处理1 m3滤液,理论上需要消耗25%的H2O2溶液________kg(用含a的代数式表示)。
②写出由Fe(OH)3制取Na2FeO4的化学方程式:_____________。
(1)2Al+2H2O+2NaOH===2NaAlO2+3H2↑ Al2O3+2NaOH===2NaAlO2+H2O
(2)2Fe3++Fe===3Fe2+(或2Fe3++Cu===2Fe2++Cu2+或Fe+Fe2O3+6H+===3Fe2++3H2O等)
(3)2Cu+O2+4H+2Cu2++2H2O
(4)①68a ②2Fe(OH)3+3NaClO+4NaOH===2Na2FeO4+3NaCl+5H2O
(2)2Fe3++Fe===3Fe2+(或2Fe3++Cu===2Fe2++Cu2+或Fe+Fe2O3+6H+===3Fe2++3H2O等)
(3)2Cu+O2+4H+2Cu2++2H2O
(4)①68a ②2Fe(OH)3+3NaClO+4NaOH===2Na2FeO4+3NaCl+5H2O
本题考查了Cu、Fe、Al及其化合物的性质以及氧化还原反应、化学计算等,意在考查考生运用所学知识综合分析问题的能力。(1) Al和Al2O3均与NaOH溶液发生反应。(2)Ⅰ所得固体混合物中含有的单质铁和铜均可将Fe3+还原为Fe2+。(4)①H2O2在酸性条件下可将Fe2+氧化为Fe3+,反应的离子方程式为2Fe2++H2O2+2H+===2H2O+2Fe3+,n(H2O2)=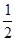 n(Fe2+)=×1000a mol=500a mol,m(H2O2)=500a mol×34 g·mol-1=17000a g,故需25%的H2O2溶液的质量为
n(Fe2+)=×1000a mol=500a mol,m(H2O2)=500a mol×34 g·mol-1=17000a g,故需25%的H2O2溶液的质量为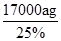 =68000a g=68a Kg。②根据化合价变化及氧化还原反应规律可知Fe(OH)3被氧化,而NaClO被还原为NaCl,然后根据得失电子守恒、原子守恒配平方程式即可。
=68000a g=68a Kg。②根据化合价变化及氧化还原反应规律可知Fe(OH)3被氧化,而NaClO被还原为NaCl,然后根据得失电子守恒、原子守恒配平方程式即可。
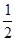 n(Fe2+)=×1000a mol=500a mol,m(H2O2)=500a mol×34 g·mol-1=17000a g,故需25%的H2O2溶液的质量为
n(Fe2+)=×1000a mol=500a mol,m(H2O2)=500a mol×34 g·mol-1=17000a g,故需25%的H2O2溶液的质量为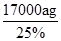 =68000a g=68a Kg。②根据化合价变化及氧化还原反应规律可知Fe(OH)3被氧化,而NaClO被还原为NaCl,然后根据得失电子守恒、原子守恒配平方程式即可。
=68000a g=68a Kg。②根据化合价变化及氧化还原反应规律可知Fe(OH)3被氧化,而NaClO被还原为NaCl,然后根据得失电子守恒、原子守恒配平方程式即可。
练习册系列答案
相关题目