题目内容
【题目】连二亚硫酸钠![]() ,俗称“保险粉”,属于一级遇湿易燃物品。
,俗称“保险粉”,属于一级遇湿易燃物品。![]() 易溶于水,难溶于乙醇,在碱性介质中可以稳定存在。如图是某兴趣小组利用锌粉法制备保险粉的装置示意图
易溶于水,难溶于乙醇,在碱性介质中可以稳定存在。如图是某兴趣小组利用锌粉法制备保险粉的装置示意图![]() 夹持、加热等装置略去
夹持、加热等装置略去![]() 。
。
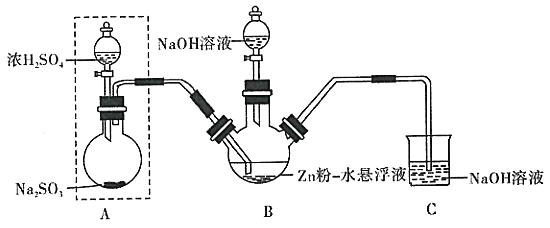
请回答有关问题:
(1)连接好仪器,检查虚线框内装置气密性良好的操作是________。A中发生反应的化学方程式为________。
(2)进入到B中的![]() 与Zn粉的水悬浮液在
与Zn粉的水悬浮液在![]() 反应生成
反应生成![]() ,需采用的加热方式为________。
,需采用的加热方式为________。
(3)将所得![]() 的悬浊液冷却至常温,加入NaOH溶液生成
的悬浊液冷却至常温,加入NaOH溶液生成![]() 和
和![]() 沉淀。欲使
沉淀。欲使![]() 沉淀完全,则需调节此溶液的pH至少为________
沉淀完全,则需调节此溶液的pH至少为________![]() 已知
已知![]() 。
。
(4)过滤出![]() 后,向所得滤液中加入适量的固体NaCl,经降温冷却、结晶过滤后再用乙醇洗涤,即可获得纯净的
后,向所得滤液中加入适量的固体NaCl,经降温冷却、结晶过滤后再用乙醇洗涤,即可获得纯净的![]() 晶体。加入固体NaCl的作用是________;用乙醇洗涤的优点是________。
晶体。加入固体NaCl的作用是________;用乙醇洗涤的优点是________。
(5)装置C的作用是________![]() 写两条
写两条![]() 。
。
(6)查阅资料:保险粉在空气中易吸收![]() 和
和![]() 生成
生成![]() 或
或![]() 和
和![]() 的混合物,请设计实验证明混合物中含有
的混合物,请设计实验证明混合物中含有![]() ,实验方案为________。
,实验方案为________。
(7)保险粉保存时应该置于________![]() 写出两项注意事项
写出两项注意事项![]() 。
。
【答案】用弹簧夹夹住乳胶管,取下分液漏斗的瓶塞,打开旋塞向漏斗中缓慢加水,若漏斗下端的水不能连续滴落,则证明气密性良好; ![]() 浓
浓![]() 水浴加热
水浴加热 ![]() 降低
降低![]() 的溶解量,便于其降温析出 降低产品因溶解而产生损耗 吸收
的溶解量,便于其降温析出 降低产品因溶解而产生损耗 吸收![]() ,防止污染空气;隔离空气,防止空气中的
,防止污染空气;隔离空气,防止空气中的![]() 将产物氧化 取少量产品溶于水,滴加少量
将产物氧化 取少量产品溶于水,滴加少量![]() 溶液,若出现白色沉淀则说明含有
溶液,若出现白色沉淀则说明含有![]() 密封、干燥、阴凉处
密封、干燥、阴凉处
【解析】
(1)利用滴液法检查装置气密性;A中浓硫酸与亚硫酸钠反应生成二氧化硫、硫酸钠和水;
(2)温度低于100![]() ,用水浴加热;
,用水浴加热;
(3)利用氢氧根离子浓度为: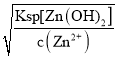 ,进行计算;
,进行计算;
(4)加入NaCl增大![]() 浓度;过滤后再用乙醇洗涤;
浓度;过滤后再用乙醇洗涤;
(5)根据装置的特点及产物的性质分析;
(6)根据离子检验方法分析;
(7)保险粉遇水都会发生反应放出大量的热,甚至引起燃烧。
(1)连接好仪器,检查装置A气密性的方法为:用弹簧夹夹住乳胶管,取下分液漏斗的瓶塞,打开旋塞向漏斗中缓慢加水,若漏斗下端的水不能连续滴落,则证明气密性良好;A中浓硫酸与亚硫酸钠反应生成二氧化硫、硫酸钠和水,发生反应的化学方程式为:![]() 浓
浓![]() ;
;
故答案为:用弹簧夹夹住乳胶管,取下分液漏斗的瓶塞,打开旋塞向漏斗中缓慢加水,若漏斗下端的水不能连续滴落,则证明气密性良好;
![]() 浓
浓![]() ;
;
(2)反应需控制温度![]() ,方法是:水浴加热;
,方法是:水浴加热;
故答案为:水浴加热;
(3)欲使![]() 沉淀完全,完全沉淀时的
沉淀完全,完全沉淀时的![]() ,
,
则完全沉淀时氢氧根离子浓度为: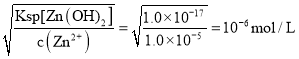 ;
;
则需调节此溶液的pH至少8;
故答案为:8;
(4)加入NaCl增大![]() 浓度,以降低
浓度,以降低![]() 的溶解量,便于其降温析出;过滤后再用乙醇洗涤,可以降低产品因溶解而产生损耗;
的溶解量,便于其降温析出;过滤后再用乙醇洗涤,可以降低产品因溶解而产生损耗;
故答案为:降低![]() 的溶解量,便于其降温析出;降低产品因溶解而产生损耗;
的溶解量,便于其降温析出;降低产品因溶解而产生损耗;
故答案为:吸收![]() ,防止污染空气;隔离空气,防止空气中的
,防止污染空气;隔离空气,防止空气中的![]() 将产物氧化;
将产物氧化;
(6)硫酸氢钠在水溶液中完全电离产生氢离子、钠离子和硫酸根离子,可以根据检验产物中是否存在硫酸根离子,具体操作为:取少量产品溶于水,滴加少量![]() 溶液,若出现白色沉淀则说明含有
溶液,若出现白色沉淀则说明含有![]() ;
;
故答案为:取少量产品溶于水,滴加少量![]() 溶液,若出现白色沉淀则说明含有
溶液,若出现白色沉淀则说明含有![]() ;
;
(7)保险粉遇水都会发生反应放出大量的热,甚至引起燃烧,故需密封、阴凉处保存;
故答案为:密封、阴凉处保存。

【题目】随着科技的进步,合理利用资源、保护环境成为当今社会关注的焦点。甲胺铅碘(CH3NH3PbI3)用作全固态钙钛矿敏化太阳能电池的敏化剂,可由CH3NH2、PbI2及HI为原料合成,回答下列问题:
(1)制取甲胺的反应为CH3OH(g)+NH3(g)CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
共价键 | C—O | H—O | N—H | C—N | C—H |
键能/kJ·mol-1 | 351 | 463 | 393 | 293 | 414 |
则该反应的ΔH=_________kJ·mol-1。
(2)上述反应中所需的甲醇工业上利用水煤气合成,反应为CO(g)+2H2(g) CH3OH(g) ΔH <0。在一定条件下,将1 mol CO和2 mol H2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
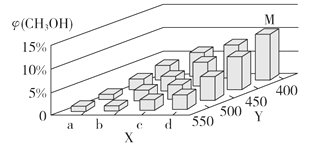
①平衡时,M点CH3OH的体积分数为10%,则CO的转化率为_________。
②X轴上a点的数值比b点_________ (填“大”或“小”)。某同学认为上图中Y轴表示温度,你认为他判断的理由是________________________________。
(3)工业上可采用CH3OH CO+2H2的方法来制取高纯度的CO和H2。我国学者采用量子力学方法,通
CO+2H2的方法来制取高纯度的CO和H2。我国学者采用量子力学方法,通
过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。
甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式 A:CH3OH* →CH3O* +H* Ea= +103.1kJ·mol-1
方式 B:CH3OH* →CH3* +OH* Eb= +249.3kJ·mol-1
由活化能E值推测,甲醇裂解过程主要历经的方式应为_________(填A、B)。
下图为计算机模拟的各步反应的能量变化示意图。
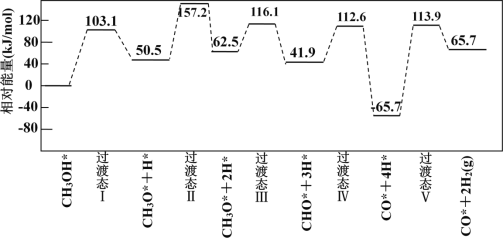
该历程中,放热最多的步骤的化学方程式为______________________________________________。
(4)常温下,PbI2饱和溶液(呈黄色)中c(Pb2+)=1.0×10-3 mol·L-1,则Ksp(PbI2)=_________。
【题目】下列实验操作能达到相应实验目的的是
选项 | 实验目的 | 实验操作 |
A | 探究I-与Fe2+的还原性强弱 | 向FeCl3稀溶液中依次加入KI溶液、淀粉 |
B | 探究HPO42-在水溶液中的电离程度与水解程度的相对大小 | 测定0.1 mol·L-1NaH2PO4溶液的pH |
C | 配制0.1 mol·L-1邻苯二甲酸氢钾( | 称取5.1 g邻苯二甲酸氢钾于烧杯中,加入少量蒸馏水溶解,转移至500 mL容量瓶中定容 |
D | 比较CaCO3和CaSO4的Ksp大小 | 向澄清石灰水中滴入0.1 mol·L-1Na2CO3溶液至不再有沉淀产生,再滴加0.1 mol·L-1Na2SO4溶液 |
A.AB.BC.CD.D

