题目内容
(1)在1-18号元素中,能形成最稳定气态氢化物的元素是 ;与水或酸反应最剧烈的金属单质是 ;最高价氧化物的水化物中碱性最强的元素是 ;最高价氧化物的水化物中酸性最强的元素是 .(填写元素符号)
(2)物质在下列变化过程中克服的是:a分子间作用力 b共价键 c离子键(填序号)
①冰融化 ; ②食盐熔化 ;
③H2S受热分解成S和H2 ; ④NaHSO4溶解于水 ;
(3)共价键、离子键和分子间作用力是构成物质的微粒间的不同作用方式,下列物质中,只含有上述一种作用的是
A.干冰 B.氯化钠 C.氢氧化钠 D.碘
(4)氮化钠是科学家制备的一种重要的化合物,它与水作用可产生NH3.请回答,Na3N的电子式是 ,Na3N与盐酸反应方程式 .
(2)物质在下列变化过程中克服的是:a分子间作用力 b共价键 c离子键(填序号)
①冰融化
③H2S受热分解成S和H2
(3)共价键、离子键和分子间作用力是构成物质的微粒间的不同作用方式,下列物质中,只含有上述一种作用的是
A.干冰 B.氯化钠 C.氢氧化钠 D.碘
(4)氮化钠是科学家制备的一种重要的化合物,它与水作用可产生NH3.请回答,Na3N的电子式是
考点:位置结构性质的相互关系应用,电子式,不同晶体的结构微粒及微粒间作用力的区别
专题:元素周期律与元素周期表专题,化学键与晶体结构
分析:(1)1~18号中,与水反应最剧烈的金属是最活泼的金属,是Na;非金属性最强的元素的气态氢化物最稳定;非金属性越强,元素的最高价氧化物对应水化物的酸性越强,F无正化合价;
(2)活泼金属和活泼非金属元素之间易形成离子键、非金属元素之间易形成共价键,分子晶体状态发生变化时会破坏范德华力,电解质溶于水会导致化学键被破坏,离子晶体熔融时会导致离子键被破坏,物质发生化学反应时有化学键的破坏和形成;
(3)一般金属元素与非金属元素之间形成离子键,非金属元素之间形成共价键,分子之间存在分子间作用力,以此来解答;
(4)Na3N与盐酸反应生成氯化钠和氯化铵.
(2)活泼金属和活泼非金属元素之间易形成离子键、非金属元素之间易形成共价键,分子晶体状态发生变化时会破坏范德华力,电解质溶于水会导致化学键被破坏,离子晶体熔融时会导致离子键被破坏,物质发生化学反应时有化学键的破坏和形成;
(3)一般金属元素与非金属元素之间形成离子键,非金属元素之间形成共价键,分子之间存在分子间作用力,以此来解答;
(4)Na3N与盐酸反应生成氯化钠和氯化铵.
解答:
解:(1)能形成最稳定气态氢化物的元素是F,1~18号中,与水反应最剧烈的金属是Na;气态氢化物最稳定的是HF;最高价氧化物的水化物中碱性最强的是NaOH,最高价氧化物所对应的水化物其酸性最强的是 HClO4;
故答案为:F;Na; Na; Cl;
(2)①冰为分子晶体,熔化时克服分子间作用力;
②食盐为离子晶体,融化时克服离子键;
③H2S受热分解,克服共价键;
④NaHSO4溶解于水,电离出钠离子、氢离子和硫酸根离子,共价键和离子键断裂,
故答案为:a;c;b;bc;
(3)A.干冰分子间存在分子间作用力,分子内存在共价键,故A错误;
B.氯化钠为离子晶体,只含有离子键,故B正确;
C.氢氧化钠含有离子键和共价键,故C错误;
D.碘分子间存在分子间作用力,分子内存在共价键,故D错误;
故答案为:B;
(4)Na3N的电子式为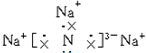 ,Na3N与盐酸反应生成氯化钠和氯化铵,反应的化学方程式为Na3N+4HCl=3NaCl+NH4Cl,
,Na3N与盐酸反应生成氯化钠和氯化铵,反应的化学方程式为Na3N+4HCl=3NaCl+NH4Cl,
故答案为: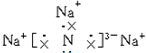 ;Na3N+4HCl=3NaCl+NH4Cl.
;Na3N+4HCl=3NaCl+NH4Cl.
故答案为:F;Na; Na; Cl;
(2)①冰为分子晶体,熔化时克服分子间作用力;
②食盐为离子晶体,融化时克服离子键;
③H2S受热分解,克服共价键;
④NaHSO4溶解于水,电离出钠离子、氢离子和硫酸根离子,共价键和离子键断裂,
故答案为:a;c;b;bc;
(3)A.干冰分子间存在分子间作用力,分子内存在共价键,故A错误;
B.氯化钠为离子晶体,只含有离子键,故B正确;
C.氢氧化钠含有离子键和共价键,故C错误;
D.碘分子间存在分子间作用力,分子内存在共价键,故D错误;
故答案为:B;
(4)Na3N的电子式为
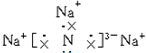 ,Na3N与盐酸反应生成氯化钠和氯化铵,反应的化学方程式为Na3N+4HCl=3NaCl+NH4Cl,
,Na3N与盐酸反应生成氯化钠和氯化铵,反应的化学方程式为Na3N+4HCl=3NaCl+NH4Cl,故答案为:
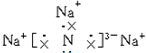 ;Na3N+4HCl=3NaCl+NH4Cl.
;Na3N+4HCl=3NaCl+NH4Cl.
点评:本题考查化学键、化学方程式的书写及电子式等知识,题目难度不大,为基础性试题的考查,试题基础性强,注重能力训练,该题有利于巩固学生对教材基础知识的理解,培养学生的规范答题能力,提高学习效率.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
下列物质中,不属于羧酸类的是( )
| A、乙二酸 | B、苯甲酸 |
| C、硬脂酸 | D、石炭酸 |
用惰性电极电解下列溶液,其中随着电解的进行,溶液pH值逐渐减小的是( )
①氯化钠溶液 ②硫酸铜溶液 ③氢氧化钠溶液 ④稀硫酸 ⑤稀盐酸 ⑥硫酸钠溶液.
①氯化钠溶液 ②硫酸铜溶液 ③氢氧化钠溶液 ④稀硫酸 ⑤稀盐酸 ⑥硫酸钠溶液.
| A、①③⑤ | B、②④⑤ |
| C、②④ | D、②④⑥ |
下列粒子半径之比大于1的是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
 有机物的结构简式为(如图),试判断它具有的官能团:
有机物的结构简式为(如图),试判断它具有的官能团: