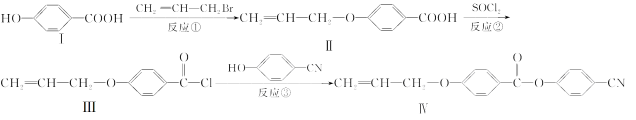
题目内容
【题目】海洋是一个巨大的物质资源和能量宝库,世界各国都在研究如何充分利用海洋资源。
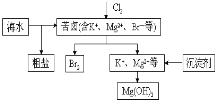
Ⅰ. 从海水中可以提取食盐。
Ⅱ.从海水中提取镁。已知MgO、MgCl2的熔点分别为2800℃、604℃,从海水中提
取镁,最合理的方法是 。
A.海水![]() Mg(OH)2
Mg(OH)2![]() Mg
Mg
B.海水![]() MgCl2溶液→MgCl2熔融
MgCl2溶液→MgCl2熔融![]() Mg
Mg
C.海水![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO![]() Mg
Mg
D.海水![]() Mg(OH)2
Mg(OH)2![]() MgCl2溶液→MgCl2熔融
MgCl2溶液→MgCl2熔融![]() Mg
Mg
Ⅲ.从海水中提溴。其工业方法有:空气吹出纯碱吸收法、空气吹出SO2吸收法、溶
剂萃取法等。
(1)空气吹出纯碱吸收法。将氯气通入富含溴离子的海水中,再用空气将溴吹出,
用纯碱溶液吸收,最后用硫酸酸化,即可得到溴单质.该方法涉及的反应有:
① (写出离子方程式);
②3Br2+3CO32﹣═BrO3﹣+5Br﹣+3CO2↑;
③BrO3﹣+5Br﹣+6H+═3Br2+3H2O
(2)空气吹出SO2吸收法。该方法基本同(1),只是将溴吹出后是用SO2来吸收的,
然后再用氯气氧化即得单质溴。
写出溴与二氧化硫反应的化学方程式: 。
【答案】Ⅱ.D
Ⅲ.(1)Cl2+2Br- =2Cl-+Br2;
(2)Br2+SO2+2H2O===H2SO4+2 HBr。
【解析】
试题分析:Ⅱ.A.在海水苦卤中加氢氧化钠过滤得沉淀氢氧化镁,Mg(OH)2热稳定性差,受热分解,故A错误;B.海水中含有可溶性的Mg2+、Ca2+、Fe3+、SO42-、Na+、Cl-、加盐酸得不到纯净的氯化镁溶液,所以无法得到纯净的氯化镁固体,故B错误;C.在海水苦卤中加石灰乳过滤得沉淀氢氧化镁,灼烧得到氧化镁,但MgO的熔点为2800℃、熔点高,电解时耗能高,所以,工业上,电解熔融MgCl2冶炼金属镁,故C错误;D.在海水苦卤中加石灰乳过滤得沉淀氢氧化镁,再将沉淀分离后加入盐酸变成MgCl2,之后经过滤、干燥、电解,即可得到金属镁,故D正确。
故答案为:D
Ⅲ.(1)氯气有强氧化性,能氧化溴离子生成溴单质,自身被还原生成氯离子,离子反应方程式为:Cl2+2Br-=Br2+2Cl-。
故答案为:Cl2+2Br- =2Cl-+Br2;
(2)溴有氧化性,二氧化硫有还原性,在水溶液里,二氧化硫和溴发生氧化还原反应生成硫酸和氢溴酸,反应方程式为:Br2+SO2+2H2O=2HBr+H2SO4。
故答案为:Br2+SO2+2H2O===H2SO4+2 HBr。

【题目】氮及其化合物在工业生产和国防建设中有广泛应用。回答下列问题:
(1)氮气性质稳定,可用作保护气。请用电子式表示氮气的形成过程: 。
(2)联氨(N2H4)是一种还原剂。已知:H2O(l)=H2O(g)△H=+44kJ/mol。试结合下表数据,写出N2H4 (g)燃烧热的热化学方程式: 。
化学键 | N—H | N—N | N=N | N≡N | O=O | O—H |
键能(kJ/mol) | 390.8 | 193 | 418 | 946 | 497.3 | 462.8 |
(3)KCN可用于溶解难溶金属卤化物。将AgI溶于KCN溶液中,形成稳定的Ag(CN)2-,该转化的离子方程式为: 。若已知Ksp(AgI)=1.5×10-16,K稳Ag(CN)2-]=1.0×1021,则上述转化方程式的平衡常数K= 。(提示:K稳越大,表示该化合物越稳定)
(4)氨的催化氧化用于工业生产硝酸。该反应可设计成新型电池,试写出碱性环境下,该电池的负极电极反应式: 。
(5)将某浓度的NO2气体充入一恒容绝热容器中,发生反应2NO2![]() N2O4其相关图像如下。
N2O4其相关图像如下。
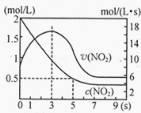
①0~3s时v(NO2)增大的原因是 。
②5s时NO2转化率为 。