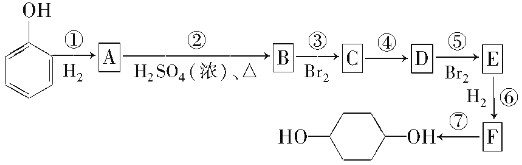
题目内容
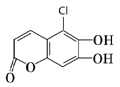
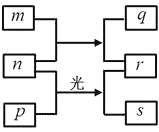
【题目】短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01 mol·L–1r溶液的pH为2,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是( )
A. 原子半径的大小W<X<Y
B. 元素的非金属性Z>X>Y
C. Y的氢化物常温常压下为液态
D. X的最高价氧化物的水化物为强酸
【答案】C
【解析】试题分析:短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,则Z是氯元素,n是Cl2;0.01 mol·L–1r溶液的pH为2,说明r是一元强酸,Cl2与两种元素组成的化合物反应会产生两种化合物,其中一种r是HCl,另一种物质q的水溶液具有漂白性,则说明W是H元素;m是H2O,q是HClO;两种元素组成的化合物p与Cl2光照反应产生HCl,同时产生s,s通常是难溶于水的混合物,根据转化关系图可知p是甲烷,则s可能是CH3Cl、CH2Cl2、CHCl3、CCl4中的几种物质。因此X是碳元素,Y是氧元素。A.根据元素周期律的原子半径变化规律:同一周期的元素,原子序数越大原子半径越小,同一主族的元素,原子核外电子层数越多,原子半径越大,则原子半径的大小W<Y<X,错误;B.同周期元素,随着原子序数的增大,自左向右元素的非金属性逐渐增强,则非金属性Y>X,最高价氧化物对应的水化物酸性越强,相应元素的非金属性越弱,高氯酸的酸性大于碳酸的酸性,则非金属性Z>X,氯元素与氧元素组成的常见化合物如次氯酸等,氯元素显正价,氧元素显负价,由此可判断非金属性Y>Z,因此元素的非金属性Y>Z>X,错误;C.Y元素的氢化物有H2O和H2O2,二者在常温常压下都为液态,正确;D.X的最高价氧化物的水化物是碳酸,该物质是二元弱酸,不是强酸,错误。

【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
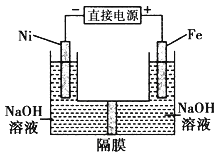
(1)Fe还原水体中NO3-的反应原理如图所示。
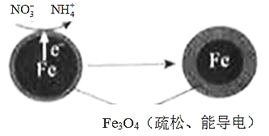
①作负极的物质是________。
②正极的电极反应式是_________。
(2)将足量铁粉投入水体中,经24小时测定NO3—的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3—的去除率 | 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
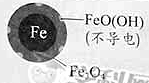
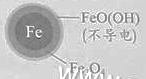
铁的最终物质形态 |
|
|
pH=4.5时,NO3—的去除率低。其原因是________。
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3—的去除率。对Fe2+的作用提出两种假设:
Ⅰ. Fe2+直接还原NO3—;
Ⅱ. Fe2+破坏FeO(OH)氧化层。
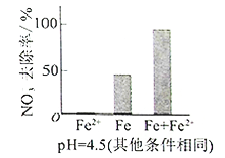
①做对比实验,结果如图所示,可得到的结论是_______。
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4。结合该反应的离子方程式,解释加入Fe2+提高NO3—去除率的原因:______。
(4)其他条件与(2)相同,经1小时测定NO3—的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3—的去除率 | 约10% | 约3% |
1小时pH | 接近中性 | 接近中性 |
与(2)中数据对比,解释(2)中初始pH不同时,NO3—去除率和铁的最终物质形态不同的原因:__________。