题目内容
碘是人体必需的微量元素之一,有“智力元素”之称。食用加碘食盐可预防碘缺乏病。查阅资料知:①在酸性条件下,I—能被NO3-离子氧化成IO3-离子,被H2O2或O2等氧化成I2;②IO3-离子能被HSO3-离子还原成I2。
请你利用实验室常用仪器和下列限选试剂,依次研究某食盐样品中所加碘的存在形式是I2、I-、IO3-中的哪一种。
限选试剂如下:1.0 mol?L-1HNO3溶液、1.0 mol?L-1 H2SO4溶液、1.0 mol?L-1NaHSO3溶液、3% H2O2溶液、1%淀粉溶液、蒸馏水
Ⅰ.提出假设
假设1:该食盐样品中含I2 ;
假设2:该食盐样品中含I—
假设3: 。
Ⅱ.设计方案与实验探究
将适量食盐样品溶于蒸馏水制成溶液,请按要求填写下表
| 实验步骤 | 预期现象与结论 |
| 步骤1:取少量上述溶液注入试管中,滴入几滴淀粉溶液振荡。 | 若溶液显 ,则假设1成立;否则,假设1不成立,再进行步骤2 |
| 步骤2: | 若溶液显蓝色,则假设2成立,反应的离子方程式为 ;否则,假设2不成立,再进行步骤3 |
| 步骤3: | |
Ⅲ.问题与思考
纯的KIO3或KI都可以作为食用加碘盐中碘的来源。从化学角度来看,试验中添加 (填“KIO3”或“KI”)更好;理由是 。
Ⅰ.该食盐中含有IO3-
Ⅱ.实验步骤 预期现象与结论 步骤1:取少量上述溶液注入试管中,滴入几滴淀粉溶液,振荡。 若溶液显蓝色,则假设1成立;
否则,假设1不成立。再进行步骤2.步骤2:取少量上述溶液注入试管中,加入适量1.0mol/LH2SO4酸化的3%H2O2溶液,再滴入几滴淀粉溶液,振荡。 若溶液显蓝色,则假设2成立,反应的离子方程式为2I-+H2O2+2H+=I2+2H2O
否则,假设2不成立。再进行步骤3.步骤3:取少量上述溶液注入试管中,加入适量1.0mol/L的NaHSO,再滴入几滴淀粉溶液,振荡。 若溶液显蓝色,则假设3成立;
否则,假设3不成立。
Ⅲ.KI不利于保存,因为KI易被空气中的氧气氧化成I2;
解析试题分析:本题以碘及碘的化学物的性质进行探究。从氧化还原反应的价态律中最低价态只有还原性,高价态具有氧化性。碘单质遇淀粉后变蓝色进行探究。解题的关键在几个氧化还原反应,如碘离子遇强氧化剂氧化为碘单质,碘离子和碘酸根发生归中反应生成碘单质进行分析,得到结论。
考点:本题以探究实验为基础,考查探究实验的基本方法,氧化还原反应基本理论,和实验基本操作方法等。

 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
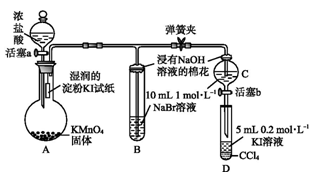
全优测试卷系列答案研究氧化还应常用到高锰酸钾,高锰酸钾是一种重要的化学试剂。为了增强其氧化性常将其酸化,但在酸性条件下其水溶液不很稳定,会分解生成二氧化锰和氧气,而在中性或弱碱性溶液中分解速度很慢,见光分解速度加快。
(1)高锰酸钾溶液保存的注意事项______________________________________________。
酸性溶液中高锰酸钾分解的离子方程式 _______________________________________。
(2)草酸可使酸性高锰酸钾溶掖褪色,请写出此反应的离子方程式______________________。
(3)某学习小组为了探究高锰酸钾溶液和草酸钠溶液的反应过程,将高锰酸钾溶液逐滴地滴入一定体积的酸性草酸钠溶液中(温度相同,并不断振荡时),记录的现象如下表:
| 滴入 KMnO4认溶液的次序(每滴溶液等体积) | KMnO4溶液紫色褪去的时间 |
| 先滴入第 1 滴 | 1min |
| 褪色后再滴入第 2 滴 | 15s |
| 褪色后再滴入第 3 滴 | 3s |
| 褪色后再滴入第 4 滴 | 1s |
请分析高锰酸钾溶液褪色时间变化的原因________________________________________。
(4)该学习小组在获取了上述经验和结论以后,用稳定的物质草酸钠来标定高锰酸钾济液的浓度。他们准确称取2.680g纯净的草酸钠配成500mL溶液,每次准确量取25.00mL溶液酸化后用KMnO4溶液滴定。
①高锰酸钾溶液应装在______(填下途中的仪器编号)。
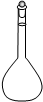


甲 乙 丙 丁
②为了防止高锰酸钾在酸性条件下分解而造成误差,滴定开始时,操作上必须是______________。
③当溶液呈微红色且半分钟内不褪色,消耗KMnO4溶液20.00mL(多次测定的平均值),则KMnO4溶液的浓度为________________。
(附原子相对质量K=39Mn=55O=16 Na=23C=12)
某化学学习小组欲探究铁及其化合物的氧化性和还原性。请你协助他们完成实验报告。
(1)实验目的:探究铁及其化合物的氧化性和还原性
(2)实验试剂及仪器:
试剂:氯化亚铁溶液、氯化铁溶液、氯水、KSCN溶液、铁粉、锌片、铜片、稀硫酸
仪器:胶头滴管外,你认为本实验必不可少的一种玻璃仪器是 。
| 序号 | 实验设计 | 实验观察(主要现象) | 离子方程式 | 解释与结论 |
| ① | 在铁粉中滴 入稀硫酸 | 铁粉溶解,溶液由无 色变成浅绿色,有无 色无味的的气体生成 | Fe +2H+= H2↑+ Fe2+ | Fe具有还原性 |
| ② | 氯化亚铁溶液中滴入KSCN溶液,再加入氯水 | 滴入KSCN溶液无明 显变化,加入氯水立 即变成血红色 | | |
| ③ | 氯化亚铁溶液加 入锌片 | | Fe2++ Zn =" Fe" + Zn 2++ | |
| ④ | | | | Fe3+具有氧化性 |
(3)实验记录(在仿照①实验作答,划线部分不必填写)
(4)学习小组的同学将从本实验中获得的知识推广到其他类物质的学习,请判断下列物质既有氧化性又有还原性的是
A、Cl2 B、Na C、Mg2+ D、H2O2
(5)在实验②中,有部分同学在氯化亚铁溶液中滴入KSCN溶液后,就出现了血红色,你认为是什么原因: ;
你将对实验员在配制氯化亚铁溶液时,提出的建议是 。
(6)在配制氯化铁溶液时,由于实验员失误,可能导致溶液中含有少量的Fe2+,为帮助实验员进行检验少量Fe2+的存在,请从下列物质中选择合适的试剂( )
A、KSCN溶液 B、稀盐酸 C、KMnO4溶液 D、NaOH溶液
25℃、101kPa下:①2Na(s)+1/2O2(g)=Na2O(s) △H1=-414kJ·mol-1
②2Na(s)+O2(g)=Na2O2(s) △H2=-511kJ·mol-1
下列说法正确的是( )
| A.①和②产物的阴阳离子个数比不相等 |
| B.①和②生成等物质的量的产物,转移电子数不同 |
| C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
| D.25℃、101kPa下,Na2O2(s)+2Na(s)=2Na2O(s) △H=-317kJ·mol-1 |
现有一块金属钠露置于空气中一段时间,为检验该固体是否部分变质为碳酸钠,先将固体样品溶解于水得到溶液,并采取下列措施,可以实现实验目的的是
| A.测所得溶液的pH |
| B.取溶液滴入酚酞观察是否变红 |
| C.取溶液加入盐酸观察是否有气泡 |
| D.取溶液加入CuSO4观察是否有沉淀 |
下列描述的物质一定是金属单质的是
| A.能失去电子的物质 | B.能得到电子的物质 |
| C.由含11个质子的原子构成的物质 | D.能与水反应的物质 |
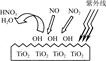
 HNO3。写出OH与NO反应的化学方程式:_____________,该反应中被氧化的元素是 。
HNO3。写出OH与NO反应的化学方程式:_____________,该反应中被氧化的元素是 。