��Ŀ����
����Ŀ����ˮ�к��зḻ��Na+��Mg2+��Cl����Br���Ȼ�ѧ��Դ������ˮ������Ũ����ˮ������ۺ����ú�ˮ��Դ��;��֮һ����Ũ����ˮΪԭ�ϣ�ͨ��һϵ�й������̿�����ȡMg��Br2�Ȳ�Ʒ��
��1����ͼ�Dz���Ĥ���뼼���ĺ�ˮ����ʾ��ͼ������Ĥ������ˮ����ͨ��������ˮ���������Ӻ����Ӿ�����ͨ������ѹ����൭ˮ�����ӵ���������ĸ���� 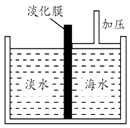
a���������� b���ܼ����� c�����ʵ���������
��2���Ӻ�ˮ����ȡþ����Ҫ�������£� 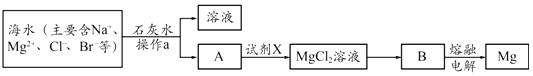
�ٲ���a�������� ��
��д��Bұ������þ�Ļ�ѧ����ʽ ��
��3�����������������ڹ�ҵ��ģ��ˮ����ij��÷���������һ�ֹ�������Ԥ�Ⱦ����ữ��Ũ����ˮΪԭ�ϣ�ͨ�����²�����ȡ�壺 ����һ���������û�������ʹ֮��Ϊ�����壻
�������ͨ�������ˮ���������崵����������ʹ�����������ռ�SO2��������ת���������
���������������������������õ���Ʒ�壮
�ٲ���һ�Ͳ������Ŀ���� ��
�ڲ�����з�����Ӧ�Ļ�ѧ����ʽΪ ��
���𰸡�
��1��b
��2�����ˣ� MgCl2�����ڣ� ![]() Mg+Cl2��
Mg+Cl2��
��3�������壻 Br2+SO2+2H2O=2HBr+H2SO4
���������⣺��1��ˮ���ӿ���������Ĥ������൭ˮ�أ�����ˮ�������������Ӳ���ͨ����ˮĤ����ѹ����൭ˮ�����ӵ����ܼ�������
���Դ��ǣ�b����2����ˮ�м���ʯ��ˮ������Ca��OH��2��þ���ӷ�Ӧ����Mg��OH��2������Ȼ��ͨ������aΪ���ˣ��õ�AΪMg��OH��2����Mg��OH��2�����Լ�XΪϡ�����еõ�MgCl2����MgCl2��Һ��HCl��Χ�����ɵõ�MgCl2���������MgCl2�õ�Mg���ʣ�
������������֪������a������Ϊ���ˣ�
���Դ��ǣ����ˣ�
��BΪ�Ȼ�þ���壬ұ������þ�Ļ�ѧ����ʽΪ��MgCl2�����ڣ� ![]() Mg+Cl2����
Mg+Cl2����
���Դ��ǣ�MgCl2�����ڣ� ![]() Mg+Cl2������3�����������û�������ʹ֮��Ϊ�����壬ͨ�������ˮ���������崵����������ʹ�����������ռ�SO2��������ת���������ᣬ����һ�Ͳ������Ŀ���Ǹ����壬
Mg+Cl2������3�����������û�������ʹ֮��Ϊ�����壬ͨ�������ˮ���������崵����������ʹ�����������ռ�SO2��������ת���������ᣬ����һ�Ͳ������Ŀ���Ǹ����壬
���Դ��ǣ������壻
�ڲ������ķ�ӦΪ��������ԭ�嵥�ʣ���Ӧ�Ļ�ѧ����ʽΪ��Br2+SO2+2H2O=2HBr+H2SO4��
���Դ��ǣ�Br2+SO2+2H2O=2HBr+H2SO4��

 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�