��Ŀ����
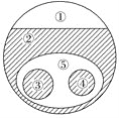
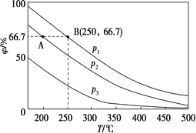
����Ŀ����������ѧ���������ҹ����в��Ų����������������ƣ�Na2S2O8������SΪ��6�ۣ�ȥ����ˮ�е��������[As(V)]���о��ɹ����䷴Ӧ����ģ����ͼ��ʾ���谢���ӵ�������ֵΪNA��Ksp[Fe(OH)3]=2.7��10��39������������ȷ���ǣ� ��
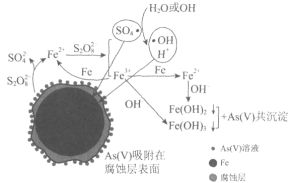
A.1mol��������(Na2S2O8)��2NA��������
B.��56gFe�μӷ�Ӧ������NA��S2O82-����ԭ
C.�����£��м����Fe(OH)3����ˮ���ñ�����Һ��c(Fe3+)Ϊ2.7��10��18mol��L��1
D.pHԽС��Խ������ȥ����ˮ�е��������
���𰸡�C
��������
A.�������ƵĽṹ��ͼ��ʾ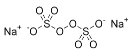 ����������ؿ�������ֻ��1����������A�����
����������ؿ�������ֻ��1����������A�����
B.һ��![]() ��һ��
��һ��![]() ��Ӧ��������
��Ӧ��������![]() ��һ��
��һ��![]() ���ù���ת��2�����ӣ�����
���ù���ת��2�����ӣ�����![]() ��Ҫ��
��Ҫ��![]() ��Ӧ���
��Ӧ���![]() �����ɻ������1mol���μӷ�ӦҪ����1.5mol
�����ɻ������1mol���μӷ�ӦҪ����1.5mol![]() ��B�����
��B�����
C.����![]() ��ע�����Һ���Լ���pH�ӽ�7����
��ע�����Һ���Լ���pH�ӽ�7����![]() �����뷽�̼��ɽ��
�����뷽�̼��ɽ��![]() Ϊ
Ϊ![]() ��C����ȷ��
��C����ȷ��
D.��Ϊ����ǽ�����ת��Ϊ���������ģ�����Һ�ļ���ԽǿԽ������������D�����
����ѡC��

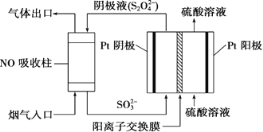
����Ŀ���ԷϾ�п�̵�س���������ѡ���ĺ��̷���(MnO2��MnOOH��MnO������Fe��Pb�ȣ�Ϊԭ���Ʊ��ߴ�MnCl2��xH2O��ʵ���̵��������á��乤���������£�
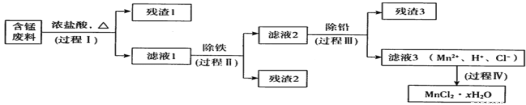
����a:Mn�Ľ������ǿ��Fe��Mn2+�����������±Ƚ��ȶ���pH����5.5ʱ�ױ�O2������
����b�������������������pH
Mn��OH��2 | Pb��OH��2 | Fe��OH��3 | |
��ʼ����ʱ | 8.1 | 6.5 | 1.9 |
��ȫ����ʱ | 10.1 | 8.5 | 3.2 |
ע���������ӵ���ʼŨ��Ϊ0.1 mol��L-l
(1)����I��Ŀ���ǽ����̡���������Һ1�к��е�������ΪMn2+��Fe3+��Pb2+��H+��
��MnO2��Ũ���ᷴӦ�����ӷ���ʽ��____________��
�ڼ�����Һ1��ֻ��Fe3+����Fe2+�IJ����������ǣ��ֱ�ȡ����������Һ1���Թ��У�һ��__________����һ�� ________________��
��Fe3+��Fe2+ת�����ɣ����ܷ����ķ�Ӧ�У�
a. 2Fe2++Cl2= 2Fe3++2Cl- b.4Fe2++O2+4H+=4Fe3++2H2O
c������ д��c�����ӷ���ʽ��____________________��
(2)���̢��Ŀ���dz��������������ַ�����
i����ˮ��������Һ1��ϡ�ͣ��ټ�����10%�İ�ˮ�����ˡ�
ii�����շ�������ҺlŨ���õ��Ĺ�����290�決�գ���ȴ��ȡ�������ˮ�ܽ⡢���ˣ���Һ�ټ������ữ������pH��
��֪�������з�������Ҫ��ӦΪ2FeCl3+3O2![]() 2Fe2O3+3Cl2������ʱMnCl2��PbCl2�������仯��
2Fe2O3+3Cl2������ʱMnCl2��PbCl2�������仯��
�ٰ�ˮ������ʱ����ҺpHӦ������__________֮�䡣
�����ַ����Ƚϣ���ˮ��������ȱ����____________��
(3)���̢��Ŀ���dz�Ǧ��������Լ���____________��
(4)���̢����ù����е�x�IJⶨ���£�ȡm1g��Ʒ�����ڵ�����Χ�м�����ʧȥȫ���ᾧˮʱ��������������m2g����x=________��