题目内容
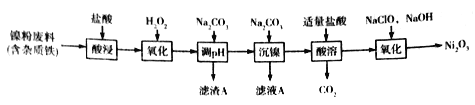
【题目】CuSO4是一种重要的化工原料,其制备途径及性质如图所示(假设恰好完全反应)。下列说法正确的是
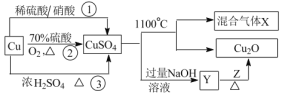
A.途径①所用混酸中,H2SO4与 HNO3物质的量之比为2:3
B.1molCuSO4在 1100℃所得混合气体中,O2为 0.75mol
C.Z 只能是葡萄糖
D.相对于途径①、③,途径②更好地体现了绿色化学思想
【答案】D
【解析】
A项、途径①的反应为铜与稀硝酸、稀硫酸反应生成硫酸铜、一氧化氮和水,反应的化学方程式为3Cu+2HNO3+3 H2SO4=3CuSO4+2NO↑+4H2O,由方程式可知混酸中H2SO4与HNO3物质的量之比最好为3:2,故A错误;
B项、CuSO4在1100℃分解生成氧化亚铜,铜元素化合价降低被还原,硫酸铜中硫元素为最高价态,只能表现氧化性,则氧元素只能被氧化化合价升高,X可能是O2和SO3或O2和SO2或O2、SO2和SO3的混合气体,若X为O2和SO3的混合气体,由得失电子数目守恒可知1molCuSO4在 1100℃所得混合气体中O2为 0.25mol,若X为O2和SO2的混合气体,由得失电子数目守恒可知1molCuSO4在 1100℃所得混合气体中O2为 0.7 5mol,若X为O2、SO2和SO3的混合气体,由得失电子数目守恒可知1molCuSO4在 1100℃所得混合气体中O2介于0.25mol 和0.7 5mol之间,故B错误;
C项、含有醛基的有机物都能与新制的氢氧化铜悬浊液共热反应生成氧化亚铜,故C错误;
D项、途径①有有害气体一氧化氮生成,途径③有有害气体二氧化硫生成,相对于途径①、③,途径②生成等量硫酸铜需要的硫酸少,无有害气体产生,更好地体现了绿色化学思想,故D正确;
故选D。

练习册系列答案
相关题目