题目内容
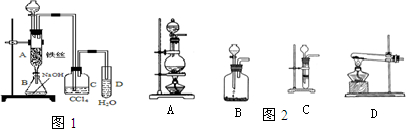
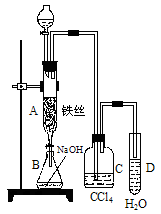
(15分)(1)某化学课外小组用右图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。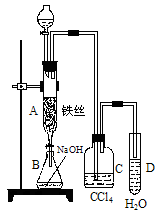
①写出A中有机反应的化学方程式 。
②已知上述有机反应是放热反应,观察到A中的现象是:
及_____ _________。
③ 实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是 ,写出有关的化学方程式 。
④C中盛放CCl4的作用是 。
⑤能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中滴入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入______ _____,现象是______________________。
(2)乙炔的实验室制法
①反应原理_____ ____________。
②选择合适的制取实验装置___ ___。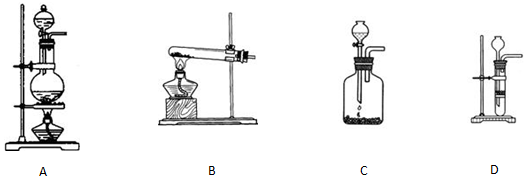
③实验中常用饱和食盐水代替水,目的是______ __________。
④纯净的乙炔气体是无色无味的气体,用电石和水反应制取的乙炔,常含有H2S和PH3而有恶臭气味。可以用____ _______溶液除去杂质气体。
(15分)(1)
① 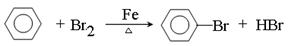
③除去溶于溴苯中的溴, Br2+2NaOH =NaBr+NaBrO+H2O
④除去溴化氢气体中的溴蒸气 ⑤石蕊试液,溶液变红色
 (2)① CaC2+2H2O C2H2↑+Ca(OH)2 ② C
(2)① CaC2+2H2O C2H2↑+Ca(OH)2 ② C ③减缓电石与水的反应速率 ④硫酸铜
解析试题分析:(1)①根据装置可知,A是制取溴苯的,反应的方程式是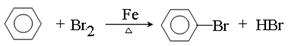 。
。
②由于反应是放热反应,而单质溴是易挥发的,所以观察到的实验现象是反应液微沸和有红棕色气体充满A容器。
③由于生成的溴苯中含有单质溴,所以实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是除去溶于溴苯中的溴,反应的方程式是Br2+2NaOH =NaBr+NaBrO+H2O。
④由于单质溴也能和硝酸银溶液反应生成白色沉淀,从而干扰溴化氢的检验,所以C中盛放CCl4的作用是除去溴化氢气体中的溴蒸气。
⑤然后是加成反应,则反应中就不会生成溴化氢,因此D中溶液不可能显酸性,据此可以鉴别。即加入石蕊试液,溶液变红色。
(2)①实验室制取乙炔是利用电石和水反应制取的,方程式是
CaC2+2H2O C2H2↑+Ca(OH)2。
C2H2↑+Ca(OH)2。
②由于反应不能加热,所以选项A和B都是错误的。电石溶于水即粉碎,所以不能用启普发生器,答案选C。
③由于电石和水的反应很剧烈,所以实验中常用饱和食盐水代替水,目的减缓电石与水的反应速率。
④H2S和PH3都能和硫酸铜溶液反应,因此可以用硫酸铜溶液除去该杂质气体。
考点:考查溴苯、乙炔的制取以及物质的除杂等。
点评:化学是一门以实验为基础的学科,所以有化学实验即科学探究之说法。纵观近几年高考,主要以考察探究性实验和物质制备实验为主。这些探究性和制备性实验的试题,综合性强,理论和实践的联系紧密,有的还提供一些新的信息,要求考生必须冷静的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能正确作答。
探究性实验的一般思路:
1、准确地把握实验目的。
2、利用已学知识,分析如何实现这个目的--实验原理。
3、结合实验材料,初步确定设计对策--实验方案。

(1)某化学课外小组用右图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
①写出A中有机反应的化学方程式
___________________________________________________
②已知上述有机反应是放热反应。观察到A中的现象是
_____________________及______________________。
③ 实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是_______________________________________________,写出有关的化学方程式____________________________________________。
④C中盛放CCl4的作用是______________________________________。
⑤能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中滴入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入__________________,现象是___________________________________________。
(2)乙炔的实验室制法
①反应原理___________________________________________________。
②选择合适的制取实验装置_______。
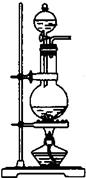

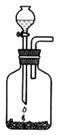 | 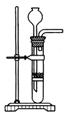 | ||
A B C D
③实验中常用饱和食盐水代替水,目的是___________________________________。
④纯净的乙炔气体是无色无味的气体,用电石和水反应制取的乙炔,常含有H2S和PH3而有恶臭气味。可以用________________溶液除去杂质气体。