题目内容
11.短周期主族元素X、Z、Y、W的原子序数依次增大.其中X、Y同主族,Y的单质是一种良好的半导体材料,Z元素原子最外层电子数等于其电子层数,W是同周期中原子半径最小的元素.下列叙述正确的是( )| A. | W-的离子半径大于Z3+的离子半径 | |
| B. | W、X形成的化合物为离子化合物 | |
| C. | X的最高价氧化物对应的水化物的酸性比W的强 | |
| D. | Y的气态简单氢化物的稳定性比X的强 |
分析 短周期主族元素X、Z、Y、W的原子序数依次增大,其中X、Y同主族,Y的单质是一种良好的半导体材料,则X为C元素、Y为Si;Z元素原子最外层电子数等于其电子层数,原子序数大于碳,只能处于第三周期,故Z为Al;W原子序数大于Si,处于第三周期,W是同周期中原子半径最小的元素,故W为Cl.
解答 解:短周期主族元素X、Z、Y、W的原子序数依次增大,其中X、Y同主族,Y的单质是一种良好的半导体材料,则X为C元素、Y为Si;Z元素原子最外层电子数等于其电子层数,原子序数大于碳,只能处于第三周期,故Z为Al;W原子序数大于Si,处于第三周期,W是同周期中原子半径最小的元素,故W为Cl.
A.Cl-离子比Al3+离子多一个电子层,故离子半径:Cl->Al3+,故A正确;
B.W、X形成的化合物为CCl4,属于共价化合物,故B错误;
C.X、W的最高价氧化物对应的水化物分别为碳酸、高氯酸,碳酸的酸性比高氯酸弱,故C错误;
D.非金属性X(C)>Y(Si),故Y的气态简单氢化物的稳定性比X的弱,故D错误,
故选A.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,注意对元素周期律的理解掌握.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
1.短周期元素X,Y,Z,W,Q在元素周期表中的相对位置如图所示.下列说法正确的是( )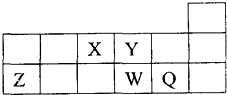

| A. | 离子Y2一和Z3+的核外电子数和核内质子数都相同 | |
| B. | 原子半径的大小顺序为:r(Z)>r(W)>r(Q)>r(Y)>r(X) | |
| C. | 最高价氧化物对应的水化物的酸性:W>Q | |
| D. | 元素X与元素Z的最高正化合价数值之和等于8 |
2.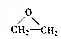 称为环氧乙烷,它在一定条件下,能与氢氧化物发生加成反应,氢原子加到氧原子上,其他部分加在碳原子上,下列对环氧乙烷的衍生物
称为环氧乙烷,它在一定条件下,能与氢氧化物发生加成反应,氢原子加到氧原子上,其他部分加在碳原子上,下列对环氧乙烷的衍生物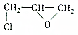 的叙述正确的是( )
的叙述正确的是( )
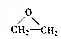 称为环氧乙烷,它在一定条件下,能与氢氧化物发生加成反应,氢原子加到氧原子上,其他部分加在碳原子上,下列对环氧乙烷的衍生物
称为环氧乙烷,它在一定条件下,能与氢氧化物发生加成反应,氢原子加到氧原子上,其他部分加在碳原子上,下列对环氧乙烷的衍生物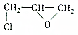 的叙述正确的是( )
的叙述正确的是( )| A. | 能与水反应生成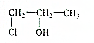 | |
| B. | 能碱性水解生成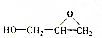 | |
| C. | 在一定条件下可以合成甘油 | |
| D. | 加入AgNO3溶液能生成难溶于硝酸的白色沉淀 |
19.矿石中金的含量很低,金的性质又相当稳定,只能用湿法冶金-氰化法提炼,即采用稀的NaOH溶液处理已粉碎的矿石,把少量的金浸取入溶液中,后用金属锌作还原剂将金从溶液中置换析出,其反应原理为:
①4Au+8NaCN+O2+2H2O═4Na[Au(CN)2]+4NaOH
②2Na[Au(CN)2]+Zn═2Au+Na2[An(CN)4]
以下有关氰化法提炼金的说法中正确的是( )
①4Au+8NaCN+O2+2H2O═4Na[Au(CN)2]+4NaOH
②2Na[Au(CN)2]+Zn═2Au+Na2[An(CN)4]
以下有关氰化法提炼金的说法中正确的是( )
| A. | Na[Au(CN)2]可溶于水 | |
| B. | 化合物Na[Au(CN)2]中金元素的化合价为+2 | |
| C. | 金化学性质稳定,不与任何物质反应 | |
| D. | 在提炼过程中含金元素的物质始终作氧化剂 |
6.下列关于乙酸的说法正确的是( )
| A. | 乙酸能够使紫色石蕊试剂变红,所以乙酸是强酸 | |
| B. | 食醋除去水垢的现象证明了酸性:乙酸>碳酸 | |
| C. | 乙酸与乙醇发生的酯化反应不属于取代反应 | |
| D. | 在制备乙酸乙酯的实验中,用18O标记乙醇,在产物乙酸乙酯中检测不到18O |
16.下列溶液物质的量浓度最大的是( )
| A. | 200mL含9.5g MgCl2的溶液 | |
| B. | 31g Na2O溶于水配成1L溶液 | |
| C. | 4%的H2SO4溶液(ρ=1.025g•cm-3) | |
| D. | 213mL 0.5mol•L-1盐酸和82mL 0.5mol•L-1盐酸的混合液 |
3.硫及其化合物有广泛应用.
(1)硫酸生产过程中涉及以下反应.已知25℃、l0l kPa时:
2SO2(g)+O2(g)+2H2O(l)═2H2SO4(l)△H=-457kJ•mol-1
SO3(g)+H2O(l)═H2SO4(l)△H=-130kJ•mol-1
则SO2催化氧化反应中,每生成l mol SO3(g)的焓变为-98.5kJ•mol-1
(2)对于SO3催化氧化反应:2SO2(g)+O2(g)?2SO3(g).
①甲图是SO2催化氧化反应时SO2(g)和SO3(g)的浓度随时间的变化情况.反应从开始到达到平衡时,用O2表示的平均反应速率为0.0375mol/(L.min).

②在一容积可变的密闭容器中充入20molSO2(g)和l0molO2(g),O2的平衡转化率随温度(T)、压强(P)的变化如图乙所示.则P1与P2的大小关系是P1< P2(填>、=或<);A、B、C三点的平衡常数大小关系是KA=KB>KC(用KA、KB、KC和>、=、<表示).
(3)为研究H2SO4生产中SO3催化氧化时温度对SO2平衡转化率的影响,进行如下试验.取100L原料气(体积分数为SO27%、O2 11%、N282%)使之发生反应,在10l kPa下达到平衡,得到如下数据:
根据上述数据,575℃达平衡时,SO3的体积分数为5.8%(保留一位小数).
(4)工业生成硫酸过程中,通常用氨水吸收尾气.
①如果相同物质的量的SO2与NH3溶于水,发生反应的离子方程式为SO2+NH3+H2O=NH4++HSO3-,所得溶液中c(H+)-c(OH-)=cd(填序号).
a.c(SO32-)-c(H2SO3)
b.c(HSO3-)+c(SO32-)-c(NH4+)
c.c(SO32-)+c(NH3•H2O)-c(H2SO3)
d.c(HSO3-)+2c(SO32-)-c(NH4+)
②工业上用足量氨水吸收硫酸工业废气.吸收SO2后的碱性溶液还可用于Cl2的尾气处理,吸收Cl2后的溶液仍呈强碱性,则吸收Cl2后的溶液中一定存在的阴离子有OH-和Cl-、SO42-.
(1)硫酸生产过程中涉及以下反应.已知25℃、l0l kPa时:
2SO2(g)+O2(g)+2H2O(l)═2H2SO4(l)△H=-457kJ•mol-1
SO3(g)+H2O(l)═H2SO4(l)△H=-130kJ•mol-1
则SO2催化氧化反应中,每生成l mol SO3(g)的焓变为-98.5kJ•mol-1
(2)对于SO3催化氧化反应:2SO2(g)+O2(g)?2SO3(g).
①甲图是SO2催化氧化反应时SO2(g)和SO3(g)的浓度随时间的变化情况.反应从开始到达到平衡时,用O2表示的平均反应速率为0.0375mol/(L.min).

②在一容积可变的密闭容器中充入20molSO2(g)和l0molO2(g),O2的平衡转化率随温度(T)、压强(P)的变化如图乙所示.则P1与P2的大小关系是P1< P2(填>、=或<);A、B、C三点的平衡常数大小关系是KA=KB>KC(用KA、KB、KC和>、=、<表示).
(3)为研究H2SO4生产中SO3催化氧化时温度对SO2平衡转化率的影响,进行如下试验.取100L原料气(体积分数为SO27%、O2 11%、N282%)使之发生反应,在10l kPa下达到平衡,得到如下数据:
| 温度/℃ | 500 | 525 | 550 | 575 | 600 |
| 平衡转化率/% | 93.5 | 90.5 | 85.6 | 80.0 | 73.7 |
(4)工业生成硫酸过程中,通常用氨水吸收尾气.
①如果相同物质的量的SO2与NH3溶于水,发生反应的离子方程式为SO2+NH3+H2O=NH4++HSO3-,所得溶液中c(H+)-c(OH-)=cd(填序号).
a.c(SO32-)-c(H2SO3)
b.c(HSO3-)+c(SO32-)-c(NH4+)
c.c(SO32-)+c(NH3•H2O)-c(H2SO3)
d.c(HSO3-)+2c(SO32-)-c(NH4+)
②工业上用足量氨水吸收硫酸工业废气.吸收SO2后的碱性溶液还可用于Cl2的尾气处理,吸收Cl2后的溶液仍呈强碱性,则吸收Cl2后的溶液中一定存在的阴离子有OH-和Cl-、SO42-.
20.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,11.2L己烷中含有分子的数目为0.5NA | |
| B. | 1mol/L CH3COOH溶液中含有CH3COOH分子的数目为NA | |
| C. | 78g 苯中含有碳碳双键的数目为3NA | |
| D. | 10g46%的乙醇水溶液中所含氢原子数目为1.2NA |
1.石蕊是一种弱酸,石蕊分子(HZ)及其酸根离子(Z-)在水溶液中具有完全不同的颜色.其中HZ的颜色是( )
| A. | 红色 | B. | 紫色 | ||
| C. | 蓝色 | D. | 视溶液的酸碱性待定H2 |