题目内容
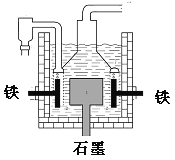
【题目】在容积为V L的某密闭容器中,a mol CO与2a mol H2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)![]() CH3OH(g)。CO的转化率与温度、压强的关系如图所示:
CH3OH(g)。CO的转化率与温度、压强的关系如图所示:
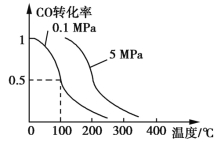
(1)该反应是 反应(填“放热”或“吸热”)。
(2)在压强为0.1 MPa条件下,200 ℃时,该反应的平衡常数K (填“=”“<”或“>”)V2/a2。
(3)在温度、容积不变的情况下,向该密闭容器再增加a mol CO(g)、2a mol H2(g)和b mol CH3OH(g),则达到新平衡时,CO的转化率 (填“增大”“减小”“不变”或“无法确定”),平衡常数 (填“增大”“减小”或“不变”)。
【答案】(1)放热 (2)< (3)无法确定 不变
【解析】(1)从题给图示可知,温度升高,CO的转化率下降,说明升温促使平衡逆向移动,正反应为放热反应。(2)在0.1 MPa压强下,100 ℃时,平衡时各物质的浓度依次为c(CO)=![]() mol·L-1=c(CH3OH),c(H2)=2c(CO)=
mol·L-1=c(CH3OH),c(H2)=2c(CO)=![]() mol·L-1,可逆反应CO(g)+2H2(g)
mol·L-1,可逆反应CO(g)+2H2(g)![]() CH3OH(g)的平衡常数K=
CH3OH(g)的平衡常数K=![]() =
=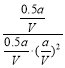 =
=![]() 。升高温度至200 ℃,平衡左移,K减小,故200 ℃时K<
。升高温度至200 ℃,平衡左移,K减小,故200 ℃时K<![]() 。(3)再加入a mol CO、2a mol H2和b mol CH3OH(g),无法确定平衡的移动,α(CO)无法确定,但温度不变,K不变。
。(3)再加入a mol CO、2a mol H2和b mol CH3OH(g),无法确定平衡的移动,α(CO)无法确定,但温度不变,K不变。

【题目】在恒容条件下,反应:2SO2 (g) + O2 (g) ![]() 2SO3(g) ΔH =-QkJ·mol-1。在上述条件下分别充入的气体和反应放出的热量 ( Q>0 )如下表所列:
2SO3(g) ΔH =-QkJ·mol-1。在上述条件下分别充入的气体和反应放出的热量 ( Q>0 )如下表所列:
容器 | SO2 (mol) | O2(mol) | N2(mol) | Q(kJ·mol-1) |
甲 | 2 | 1 | 0 | Q1 |
乙 | 1 | 0.5 | 0 | Q2 |
丙 | 1 | 0.5 | 1 | Q3 |
根据以上数据,下列叙述正确的是( )
A. 在上述条件下反应生成lmol SO3固体放热Q/2 kJ B. 2Q3 <2Q2=Q1<Q
C. Ql =2Q2= 2Q3 = Q D. 2Q2 = 2Q3 < Q1 < Q