题目内容
已知维生素A的结构简式如图.关于它的叙述正确的是( )
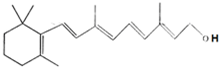

| A、维生素A的分子式为C20H30O |
| B、维生素A是一种易溶于水的醇 |
| C、维生素A分子中含有羟基、碳碳双键和苯环等官能团 |
| D、1mol维生素A最多可与7mol H2发生加成反应 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:有机物偶碳碳双键,可发生加成、加聚和氧化反应,含有羟基,可发生取代、氧化和消去反应,结合有机物结构简式可确定有机物分子式,以此解答该题.
解答:
解:A.由结构简式可知有机物的分子式为C20H30O,故A正确;
B.维生素A属于脂溶性维生素,难溶于水,故B错误;
C.苯环不是官能团,故C错误;
D.因1mol该物质含5molC=C键,则1mol维生素A分子最多可跟5molH2发生加成反应,故D错误.
故选A.
B.维生素A属于脂溶性维生素,难溶于水,故B错误;
C.苯环不是官能团,故C错误;
D.因1mol该物质含5molC=C键,则1mol维生素A分子最多可跟5molH2发生加成反应,故D错误.
故选A.
点评:本题考查有机物的结构与性质,为高考常见题型,注意把握结构中的官能团为解答的关键,熟悉烯烃、醇的性质即可解答,题目难度不大.

练习册系列答案
相关题目
钾和钠的性质相似,下列说法中能最好地解释这个事实的是( )
| A、都是金属元素 |
| B、KOH和NaOH都是强碱 |
| C、最外层电子数相同 |
| D、最高化合价相同 |
由铜制备硝酸铜,考虑到生产成本和减少污染,下列最合理的方法是( )
A、Cu
| ||
B、Cu
| ||
C、Cu
| ||
D、Cu→CuO
|
下列溶液中微粒的物质的量浓度关系正确的是( )
| A、NaHCO3溶液中存在:c(Na+)+c(H+)═c(OH-)+c(HCO3-)+c(CO32-) |
| B、室温下,向0.01mol?L-1 NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
| C、Na2CO3溶液:c(OH-)+c(HCO3-)=c(H+)+2c(H2CO3) |
| D、25℃时,Al(OH)3固体在20mL 0.01mol/L氨水中的Ksp比在20mL 0.01mol/LNH4Cl溶液中的Ksp小 |
下列说法中,正确的是( )
| A、氯气可使湿润的红色布条退色,所以氯气具有漂白性 |
| B、铁在氯气中能剧烈燃烧并产生棕黄色烟,生成FeCl2 |
| C、氯水是混合物,它跟液氯不是同一物质 |
| D、漂白粉的有效成分是NaClO,久置于空气中容易变质 |
下列关于氢键的说法正确的是( )
| A、由于氢键的作用,使NH3、H2O、HF的沸点反常,且沸点高低顺序为HF>H2O>NH3 |
| B、氢键只能存在于分子间,不能存在于分子内 |
| C、在固态水(冰)中,水分子间氢键数目增多,造成体积膨胀,密度减小 |
| D、相同量的水在气态、液态和固态时均有氢键,且氢键的数目依次增多 |
常温下,下列溶液中的微粒浓度关系正确的是( )
A、将25℃纯水加热至95℃时,
| ||
| B、pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) | ||
| C、0.2mol/L CH3COOH与0.1mol/L NaOH等体积混合:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) | ||
| D、电解NaCl溶液得到22.4L H2(标准状况),理论上需要转移NA个电子(NA表示阿伏加德罗常数) |
下列说法中错误的是( )
| A、磺化、硝化、风化、钝化都是化学变化 |
| B、蒸馏、干馏、常压分馏、减压分馏、都是物理变化 |
| C、甘油不是油,纯碱不是碱,酚醛树脂不是酯,干冰不是冰 |
| D、水煤气、裂解气、焦炉气、天然气都是混合物 |
 中和热概念:酸与碱发生中和反应生成1mol H2O时释放的热量.已知
中和热概念:酸与碱发生中和反应生成1mol H2O时释放的热量.已知