题目内容
由铜制备硝酸铜,考虑到生产成本和减少污染,下列最合理的方法是( )
A、Cu
| ||
B、Cu
| ||
C、Cu
| ||
D、Cu→CuO
|
考点:绿色化学
专题:
分析:A.Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,反应生成有毒气体;
B.3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O,反应生成有毒气体;
C.Cu+2AgNO3═Cu(NO3)2+2Ag,硝酸银比较昂贵;
D.2Cu+O2
2CuO,CuO+2HNO3=Cu(NO3)2+H2O,消耗的硝酸较少且产物没有污染.
B.3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O,反应生成有毒气体;
C.Cu+2AgNO3═Cu(NO3)2+2Ag,硝酸银比较昂贵;
D.2Cu+O2
| ||
解答:
解:A.生成1mol硝酸铜,消耗4mol硝酸,同时产生二氧化氮有毒气体,故A不选;
B.生成1mol硝酸铜,消耗
mol硝酸,同时产生一氧化氮有毒气体,故B不选;
C.反应消耗硝酸银,成本较高,故C不选;
D.生成1mol硝酸铜,消耗2mol硝酸,成本低,没有有毒气体产生,故D选;
故选:D.
B.生成1mol硝酸铜,消耗
| 8 |
| 3 |
C.反应消耗硝酸银,成本较高,故C不选;
D.生成1mol硝酸铜,消耗2mol硝酸,成本低,没有有毒气体产生,故D选;
故选:D.
点评:本题考查了铜和硝酸的性质,制备硝酸铜时应注意生产成本和环境污染,题目难度不大.

练习册系列答案
相关题目
21世纪化学的最新定义为“化学是一门创造新物质的科学”.下列有关说法不正确的是( )
| A、利用人工光合成反应,探究将二氧化碳转化为碳氢化合物作燃料,属于低碳技术 |
| B、开发安全、高效、低毒及低残留的新型农药 |
| C、大量生产聚乙烯、聚氯乙烯一次性超薄袋,方便日常生活 |
| D、制备物质时探究化学反应中高的选择性、转化率和原子利用率,属于“绿色”的生产工艺 |
下列实验现象描述错误的是( )
| A、H2在Cl2中燃烧发出苍白色火焰 |
| B、将S02通人品红溶液,溶液退色 |
| C、往稀硫酸中滴加酚酞试液,溶液变红色 |
| D、往淀粉溶液中滴加碘水,溶液显蓝色 |
常温下,下列各组离子在指定的溶液中可能大量共存的是( )
| A、无色透明溶液中:Al3+、Ca2+、Cl-、HCO3- |
| B、含大量Fe3+的溶液中:K+、I-、SO42-、NO3- |
| C、与Al反应放出H2的溶液中:NH4+、Na+、NO3-、F- |
| D、由水电离出的c(H+)=1.0×10-14mol/L的溶液中:Mg2+、K+、Cl-、SO42- |
将2mol A和2mol B通入一密闭容器中,在某温度下达到平衡:2A(g)+B(g)?2C(g)+D(g).经测定,平衡时混合气体中C的体积分数为24%,则B的转化率为( )
| A、73% | B、24% |
| C、36% | D、12% |
W、Z、Y、X四种短周期元素的原子序数依次减少.W、Z位于同周期,原子半径Z大于W;Z、W的最高正价之和等于X的最高正价;W的质子数等于X、Y的质子数之和;W的最高价氧化物对应的水化物与Z、Y的最高价氧化物对应的水化物均能发生反应.下列说法中不正确的是( )
| A、气态氢化物的稳定性:X<Y |
| B、没有X元素也就没有丰富的有机世界 |
| C、非金属性Y>X,金属性W>Z |
| D、在一定条件下,利用X、Z或W单质的还原性,可以冶炼某些金属 |
在下列分子中,能够在同一个平面内的原子数最多的是( )
| A、甲烷 |
| B、一溴甲烷(CH3Br) |
| C、乙烯 |
| D、CH2=CH-C≡CH |
已知维生素A的结构简式如图.关于它的叙述正确的是( )
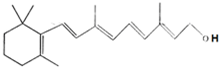

| A、维生素A的分子式为C20H30O |
| B、维生素A是一种易溶于水的醇 |
| C、维生素A分子中含有羟基、碳碳双键和苯环等官能团 |
| D、1mol维生素A最多可与7mol H2发生加成反应 |