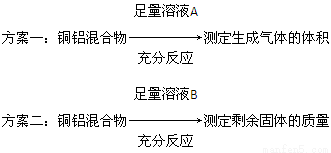
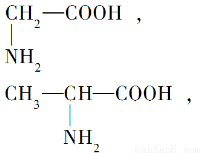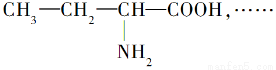题目内容
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9;单质Y和W都可与浓的NaOH溶液反应。请回答下列问题:
(1)Y、Z、W的原子半径由小到大的顺序是________(用元素符号表示)。
(2)ZW2的分子式为________________。
(3)工业生产单质Y的原理是__________________(用化学方程式表示)。
(4)X与Y化学性质相似,则X与浓的NaOH溶液反应的化学方程式是___________________________________________________。
(5)0.1 mol的单质W与50 mL 1.5 mol·L-1的FeBr2溶液反应,则被氧化的Fe2+和Br-的物质的量之比是______。
(1)Cl<S<Al
(2)SCl2
(3)2Al2O3(熔融) 4Al+3O2↑
4Al+3O2↑
(4)Be+2NaOH=Na2BeO2+H2↑
(5)3∶5
【解析】根据X为四种原子中原子序数最小的短周期元素,且X原子最外层电子数与次外层电子数相等可知,X为Be。X与W最外层电子数之和为9,且W为四种元素中原子序数最大的元素可知,W为Cl。又因为单质Y能与浓NaOH溶液反应,结合四种元素中只有两种金属元素,所以Y为Al,再根据Y与Z最外层电子数之和为9,推断Z为S。工业生产Al采用电解溶融的Al2O3的方法。Be与Al性质相似,具有两性,Be+2NaOH=Na2BeO2+H2↑。还原性强弱顺序为Fe2+>Br-,n(Cl2)=0.1 mol、n(Fe2+)=0.075 mol,n(Br-)=0.15 mol。可知Cl2能氧化全部Fe2+和部分Br-,设被氧化的Br-的物质的量为x,根据得失电子相等,0.1 mol×2=0.075 mol+x,x=0.125 mol,即n(Fe2+)∶n(Br-)=0.075 mol∶0.125 mol=3∶5。

目前世界上60%的镁是从海水中提取的。已知海水提取镁的主要步骤如下:

(1)关于加入试剂①作沉淀剂,有以下几种不同方法,请完成下列问题。
方法 | 是否正确 | 简述理由 |
方法1:直接往海水中加入沉淀剂 | 不正确 | (一) |
方法2:高温加热蒸发海水后,再加入沉淀剂 | (二) | (三) |
你认为最合理的其他方法是: (四) | ||
(一)_______________________________________________;
(二)_______________________________________________;
(三)______________________________________________;
(四)______________________________________________。
(2)框图中加入的试剂①应该是________(填化学式);加入的试剂②是________(填化学式);工业上由无水MgCl2制取镁的化学方程式为________________________________________。