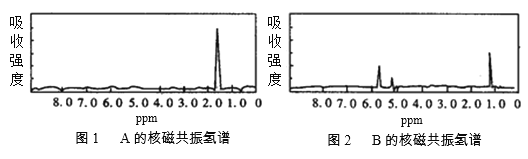
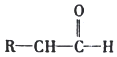题目内容
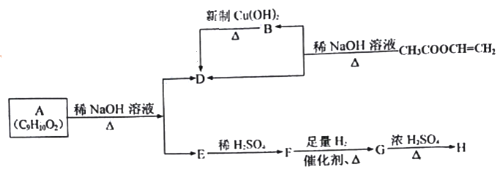
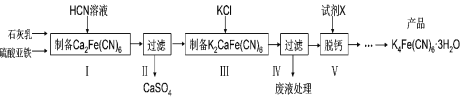
【题目】黄血盐[亚铁氰化钾,K4Fe(CN)6] 目前广泛用作食品添加剂(抗结剂),我国卫生部规定食盐中黄血盐的最大使用量为10mg/kg。一种制备黄血盐的工艺如下:
回答下列问题:
(1)步骤I反应的化学方程式为______。
(2)步骤IV过滤所得的废液中含量较多的溶质为______(填化学式)。
(3)步骤V是将难溶的K2CaFe(CN)6与X反应脱钙生成K4Fe(CN)6,所用的试剂X是_____。(填名称)
(4)工艺中用到剧毒的HCN溶液,含CN-的废水必须处理后才能排放。
①25°C时Ka(HCN)=6.25×10-10;计算25℃时0.01molL-1的HCN溶液的pH=____(lg2.5=0.4)。
②处理含CN-废水的方法:第一步控制pH>10,用NaClO溶液先将CN-不完全氧化为OCN;第二步控制pH为7.58.5,用NaClO溶液完全氧化OCN生成N2和两种盐(其中一种为酸式盐)。
第一步控制强碱性的主要目的是_______,第二步反应的离子方程式为______。
【答案】3Ca(OH)2+FeSO4+6HCN=Ca2Fe(CN)6+CaSO4+6H2O CaCl2(KCl可答,也可不答) 碳酸钾 5.6 HCl有剧毒,防止生成HCN污染环境 2OCN-+3ClO-+H2O=N2↑+3Cl-+2HCO3-
【解析】
将石灰乳、硫酸亚铁及过量HCN溶液混合可得Ca2Fe(CN)6,过滤除去含有CaSO4的滤渣,滤液中加入KCl,可得K2CaFe(CN)6沉淀,经过滤后,滤液中加入K2CO3进行脱钙处理,最终经蒸发浓缩、冷却结晶、过滤并洗涤干燥得产品K4Fe(CN)63H2O,以此来解答。
(1)步骤Ⅰ中石灰乳、硫酸亚铁及过量HCN溶液混合可得Ca2Fe(CN)6,反应的化学方程式为3Ca(OH)2+FeSO4+6HCN=Ca2Fe(CN)6+CaSO4+6H2O;
(2)步骤Ⅵ过滤所得的废液中含量较多的溶质为CaCl2(或答CaCl2、KCl);
(3)步骤V目的是进行脱钙处理,降低溶液中Ca2+的含量,所用的试剂X是K2CO3;
(4)①25°C时Ka(HCN)=6.25×10-10,根据平衡常数的含义,K=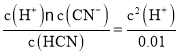 =6.25×10-10,解得c(H+)=2.5×10-6 mol/L,所以在25℃时0.01 mol/L的HCN溶液的pH =-lg2.5×10-6=6-0.4=5.6;
=6.25×10-10,解得c(H+)=2.5×10-6 mol/L,所以在25℃时0.01 mol/L的HCN溶液的pH =-lg2.5×10-6=6-0.4=5.6;
②第一步控制强碱性的主要目的是防止生成HCN,污染环境;第二步是用NaClO“不完全氧化”OCN-生成N2和两种盐,根据电子守恒、电荷守恒可知发生反应的离子方程式为2OCN-+3ClO-+H2O=N2↑+3Cl-+2HCO3-。

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案