题目内容
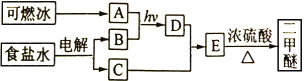
【题目】硫代硫酸钠(Na2S2O3·5H2O),又名大苏打、海波,主要用于照相业作定影剂、作鞣革时重铬酸盐的还原剂,易溶于水,遇酸易分解。其工艺制备流程如下:
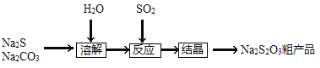
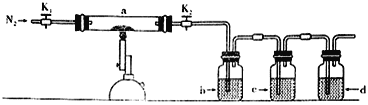
某化学兴趣小组同学模拟该流程设计了如下实验装置:
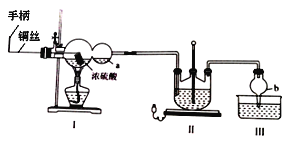
回答下列问题:
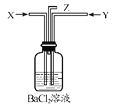
(1)双球管a处的液体可用来检验I中的反应是否发生,选用的试剂是______(填字母)
a、品红溶液 b、NaOH溶液 c、稀硫酸
若要停止I中的化学反应,除停止加热外,还要采取的操作是___________________。
(2)加热I,使反应完全,发现浸入液面下的铜丝变黑,甲同学对黑色生成物提出如下假设:①可能是Cu2O;②可能是CuO;③可能是CuS;④CuS和CuO的混合物。乙同学提出假设①一定不成立,该同学的依据是____________________________________;丙同学做了如下实验来验证黑色物质的组成:

基于上述假设分析,原黑色物质的组成为____________________(填化学式)。
(3)II中发生反应的化学方程式为_____________________,实验中通入的SO2不能过量,可能的原因是______________________________________________________。
(4)丁同学提出上述实验装置的设计存在不足,建议在I上_____________;在I、II之间增加_____________。
【答案】a 旋转手柄使铜丝螺旋部分与液面脱离 Cu2O为红色固体 CuS、CuO 2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2 过量SO2使溶液呈酸性,Na2S2O3遇酸易分解 在双球管支管口处增加一赶气装置 安全瓶(或缓冲瓶)
【解析】
从流程图中分析反应的原理,从装置图中分析实验过程中的不足之处。
(1)铜和浓硫酸加热反应生成二氧化硫气体,二氧化硫具有漂白性,检验产物二氧化硫可以用品红溶液;要想停止反应,根据图示可以旋转手柄使铜丝螺旋部分与液面脱离;故答案为:a ,旋转手柄使铜丝螺旋部分与液面脱离;
(2) Cu2O为红色固体,所以黑色物质不可能为Cu2O;硫化铜既不溶于水也不溶于硫酸;氧化铜虽然不溶于水,但是可溶于硫酸,所以与硫酸反应生成蓝色溶液和黑色固体,则该黑色物质为CuS和CuO;故答案为:Cu2O为红色固体,CuS、CuO;
(3)根据流程图II中发生反应的化学方程式为:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2;题干中提示硫代硫酸钠遇酸易分解,所以二氧化硫不能过量的原因为:过量SO2使溶液呈酸性,Na2S2O3遇酸易分解;故答案为:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2,过量SO2使溶液呈酸性,Na2S2O3遇酸易分解;
(4)从装置上看要想使生产的二氧化硫顺利进入装置II ,需要在双球管支管口处增加一赶气装置;装置I需要加热,温度比较高,为了防止倒吸情况,需要在在I、II之间增加
安全瓶(或缓冲瓶);故答案为:在双球管支管口处增加一赶气装置,安全瓶(或缓冲瓶)。

【题目】一名同学把4.48 L(已折算成标准状况下)某有机物蒸气在O2中充分燃烧,然后让产物依次通过装有无水CuSO4的干燥管、盛有浓H2SO4的洗气瓶和盛有含0.8 mol Ca(OH)2的澄清石灰水的烧杯,如图所示:
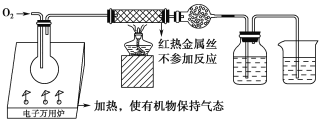
实验结束后发现无水CuSO4变蓝,干燥管和洗气瓶共增重18 g,澄清石灰水变浑浊后又恰好变澄清。请根据实验回答下列问题:
(1)O2要过量的原因是:________________。
(2)若该有机物只含C、H两种元素,且不含任何官能团,也不含脂环,则该有机物的分子式为________,它可能属于________(填序号)。
A.烷烃 B.苯的同系物 C.芳香烃 D.烃的衍生物
该物质可能的结构简式为_____________________。
(3)若该有机物分子中含有一个氧原子,则它可能是哪几类物质?请各举一例,填写在下表中:
物质种类 | 实例(写结构简式) |
_________ | _________ |
_________ | _________ |
_________ | _________ |