题目内容
19.下列装置、操作及说法正确的是( )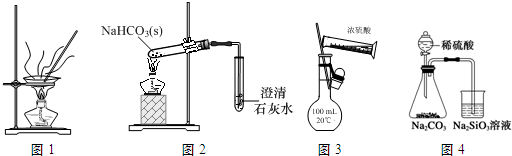
| A. | 用图1装置灼烧CuSO4•5H2O晶体除去结晶水 | |
| B. | 用图2装置探究NaHCO3的热稳定性 | |
| C. | 用图3装置配制100 mL 0.1 mol•L-1的硫酸 | |
| D. | 用图4装置比较硫、碳、硅三种元素的非金属性强弱 |
分析 A.灼烧固体用坩埚;
B.导管口应向下倾斜;
C.容量瓶不能用来稀释溶液;
D.可根据最高价氧化物的水化物的酸性比较非金属性强弱.
解答 解:A.灼烧固体用坩埚,不能用蒸发皿,故A错误;
B.导管口应向下倾斜,防止试管炸裂,故B错误;
C.容量瓶不能用来稀释溶液,应在烧杯中稀释,故C错误;
D.若锥形瓶中生成气体,说明硫酸的酸性比碳酸强,烧杯中生成白色沉淀,说明碳酸的酸性比硅酸强,最高价氧化物对应水化物酸性越强,则对应元素的非金属性越强,因此比较硫、碳、硅非金属性强弱的实验方案合理,故D正确.
故选D.
点评 本题考查较为综合,涉及物质的加热、溶液的配制、非金属性的比较等,为高考常见题型,侧重于学生的分析能力和实验能力的考查,注意把握实验的原理和操作方法,难度中等.

练习册系列答案
相关题目
13.由下列反应式所得出的结论中正确的是( )
| A. | HClO+SO2+H2O═HCl+H2SO4:酸性 HClO>H2SO4 | |
| B. | Al2O3+2NaOH═2NaAlO2+H2O:Al2O3是两性氧化物 | |
| C. | NH3+H3O+═NH4++H2O:NH3结合H+的能力比H2O强 | |
| D. | 已知C(s,石墨)═C(s,金刚石)△H=+1.9 kJ/mol:金刚石比石墨稳定 |
7.下列关于煤、天然气、石油等资源的说法不正确的是( )
| A. | 煤的干馏是化学变化 | |
| B. | 石油和天然气的主要成分都是碳氢化合物 | |
| C. | 石油裂化得到的汽油是纯净物 | |
| D. | 煤焦油的分馏可以获得各种芳香烃 |
14.我国规定饮用水质量标准必须符合下列要求:
以下是源水处理成自来水的工艺流程示意图
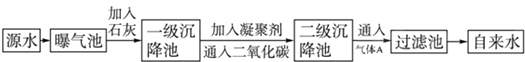
(1)源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入生石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式:Ca2++HCO-3+OH-=CaCO3↓+H2O,?Mg2++2HCO-3+2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O,Mg2++2OH-=Mg(OH)2↓..
(2)凝聚剂除去悬浮固体颗粒的过程③(填序号).FeSO4•7H2O是常用的凝聚剂,它在水中最终生成胶状Fe(OH)3沉淀.
①只是物理过程 ②只是化学过程 ③是物理和化学过程
(3)通入二氧化碳的目的是除去除去Ca2+和调节PH值.
(4)气体A的作用是强氧化.这种作用是基于气体A和水反应的产物具有Cl2+H2O=H++Cl-+HClO性.
(5)下列物质中①③可以作为气体A的代用品.
①Ca(ClO)2 ②NH3(液) ③K2FeO4 ④SO2.
| pH | 6.5~8.5 |
| Ca2+、Mg2+ | <0.004 5mol•L-1 |
| 细菌总数 | <100个/mL |

(1)源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入生石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式:Ca2++HCO-3+OH-=CaCO3↓+H2O,?Mg2++2HCO-3+2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O,Mg2++2OH-=Mg(OH)2↓..
(2)凝聚剂除去悬浮固体颗粒的过程③(填序号).FeSO4•7H2O是常用的凝聚剂,它在水中最终生成胶状Fe(OH)3沉淀.
①只是物理过程 ②只是化学过程 ③是物理和化学过程
(3)通入二氧化碳的目的是除去除去Ca2+和调节PH值.
(4)气体A的作用是强氧化.这种作用是基于气体A和水反应的产物具有Cl2+H2O=H++Cl-+HClO性.
(5)下列物质中①③可以作为气体A的代用品.
①Ca(ClO)2 ②NH3(液) ③K2FeO4 ④SO2.
4.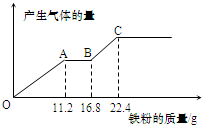 取某稀硫酸和稀硝酸的混合溶液100mL.向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸被还原为NO气体).下列分析或结果正确的是( )
取某稀硫酸和稀硝酸的混合溶液100mL.向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸被还原为NO气体).下列分析或结果正确的是( )
 取某稀硫酸和稀硝酸的混合溶液100mL.向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸被还原为NO气体).下列分析或结果正确的是( )
取某稀硫酸和稀硝酸的混合溶液100mL.向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸被还原为NO气体).下列分析或结果正确的是( )| A. | 最终溶液中所含的溶质为FeSO4 | |
| B. | OA段产生的气体是H2,BC段产生的气体是NO | |
| C. | 整个反应中转移电子数为1.2mol | |
| D. | 混合酸中NO3-的物质的量为0.2 mol |
11.如图为KNO3、NaCl的溶解度曲线图,下列有关说法正确的是( )


| A. | 温度相同(>t1℃)时,KNO3溶液中溶质的质量分数大于NaCl溶液中溶质的质量分数 | |
| B. | t1℃时,KNO3、NaCl饱和溶液中溶质的物质的量浓度相等 | |
| C. | 用“溶解→蒸发→趁热过滤”方法可提纯含有少量KNO3杂质的NaCl固体 | |
| D. | 将50g KNO3饱和溶液从t2℃降至t1℃,析出固体质量小于0.5(b-a)g |
8.下列物质①C2H6 ②C3H6 ③C6H14 ④C5H8充分燃烧,等质量时产生CO2最多的、消耗O2最多的;等物质的量时消耗O2最多的、生成水最多的依次是( )
| A. | ④①③① | B. | ④①③③ | C. | ④③④③ | D. | ①②④③ |
9.用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 5.6g金属铁与足量稀盐酸反应完全反应时,失去0.3NA个电子 | |
| B. | 20g重水(2H2O)含有10NA个电子 | |
| C. | 0.1mol/L的氯化铝溶液500mL,氯离子的物质的量浓度为0.15 mol/L | |
| D. | 在常温常压下,11.2 L氮气所含的原子数目为NA |
 ).
).
 .
.