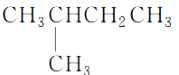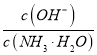题目内容
【题目】阿伏加德罗常数约为6.02×![]()
![]() ,下列叙述不正确的是( )
,下列叙述不正确的是( )
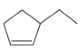
A.将1 mol ![]() 转化为
转化为![]() 胶体,
胶体,![]() 胶粒数小于6.02×
胶粒数小于6.02×![]()
B.标准状况下,22.4 L![]() 中含有溴原子数约为2×6.02×
中含有溴原子数约为2×6.02×![]()
C.常温下,9.2 g ![]() 含有的分子数小于0.2×6.02×
含有的分子数小于0.2×6.02×![]()
D.25℃时,pH=12的![]() 溶液1 L所含
溶液1 L所含![]() 数约为6.02×
数约为6.02×![]()
【答案】BD
【解析】
A.因胶体粒子是由多个Fe (OH)3离子对聚合而成,共1molFe(OH)3胶粒的物质的量小于1mol,胶粒数小于6.02×![]() ,故A正确;
,故A正确;
B.标准状况下,![]() 是液体,不能使用标况下气体的摩尔体积进行计算,故B错误;
是液体,不能使用标况下气体的摩尔体积进行计算,故B错误;
C.9.2 g ![]() 的物质的量n=
的物质的量n=![]() =
=![]() =0.2mol,由于二氧化氮会和四氧化二氮相互转化,含有分子数小于N=nNA=0.2×6.02×
=0.2mol,由于二氧化氮会和四氧化二氮相互转化,含有分子数小于N=nNA=0.2×6.02×![]() ,故C正确;
,故C正确;
D.25℃时,水的离子积常数Kw=10-14,pH=12,c(H+)=10-12 mol/L,c(OH-)=![]() =0.01mol/L,V=1L,n(OH-)=c(OH-)V=0.01 mol/L×1L=0.01mol,氢氧化钠是强电解质,电离出1mol氢氧根离子就电离出1mol钠离子,故钠离子的数目为N=nNA=0.01×6.02×
=0.01mol/L,V=1L,n(OH-)=c(OH-)V=0.01 mol/L×1L=0.01mol,氢氧化钠是强电解质,电离出1mol氢氧根离子就电离出1mol钠离子,故钠离子的数目为N=nNA=0.01×6.02×![]() =6.02×1021,故D错误;
=6.02×1021,故D错误;
答案选BD。

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
【题目】下列①②对应的试剂(或条件)不能完成实验目的的是( )
![]()
实验目的 | 试剂(条件) | |
A | 温度对Na2S2O3溶液与H2SO4溶液反应速率的影响 | ①热水浴②冷水浴 |
B | 用Na块检验乙醇分子存在不同于烃分子里的氢原子 | ①乙醇②煤油 |
C | 用硝酸酸化的AgNO3溶液检验自来水中能否蒸馏除去Cl- | ①自来水②蒸馏水 |
D | 催化剂对H2O2分解速率的影响 | ①0.1mol/LFeCl3 ②0.2mol/LFeCl3 |
A.AB.BC.CD.D