题目内容
【题目】某兴趣小组在实验室用加热乙醇、浓H2SO4、溴化钠和少量水的混合物来制备溴乙烷,检验反应的部分副产物,并探究溴乙烷的性质。
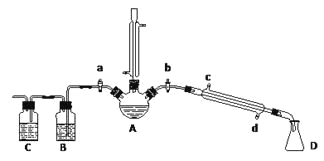
(一)溴乙烷的制备及产物的检验:设计了如上图装置,其中夹持仪器、加热仪器及冷却水管没有画出。请根据实验步骤,回答下列问题:
(1)仪器A的名称是_________
(2)制备操作中,加入少量的水,其目的是_______。(填字母)
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(3)加热片刻后,A中的混合物出现橙红色,该橙红色物质可能是____________
(4)理论上,上述反应的副产物还可能有:乙醚(CH3CH2-O-CH2CH3)、乙烯、溴化氢等
① 检验副产物中是否含有溴化氢:熄灭酒精灯,在竖直冷凝管上方塞上塞子、打开a,利用余热继续反应直至冷却,通过B、C装置检验。B、C中应盛放的试剂分别是_______、_________
② 检验副产物中是否含有乙醚:通过红外光谱仪鉴定所得产物中含有“-CH2CH3”基团,来确定副产物中存在乙醚。请你对该同学的观点进行评价:________________
(5)欲除去溴乙烷中的少量杂质Br2,下列物质中最适合的是________。(填字母)
a.NaI b.NaOH c.NaHSO3 d.KCl
(二)溴乙烷性质的探究:
用右图实验装置(铁架台、酒精灯略) 验证溴乙烷的性质:

Ⅰ:在试管中加入10 mL6mol/L NaOH溶液和2 mL 溴乙烷,振荡。
II:将试管如图固定后,水浴加热。
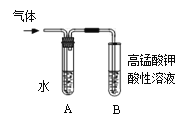
(1)观察到___________现象时,表明溴乙烷与NaOH溶液已完全反应。
(2)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,将生成的气体通入如图装置。A试管中的水的作用是______________,若无A试管,B试管中的试剂应为_____________。
【答案】三颈烧瓶 abc Br2 苯(或四氯化碳等有机溶剂) 硝酸银或石蕊试液 不正确,溴乙烷中也含乙基 c 液体不分层 吸收乙醇 溴水
【解析】
(一)在实验室用加热乙醇、浓H2SO4、溴化钠和少量水的混合物来制备溴乙烷,原理是CH3CH2OH+HBr→CH3CH2Br+H2O,HBr有浓硫酸和溴化钠反应制得。但是浓硫酸具有强氧化性,会氧化-1价的溴,所以需要加入少量水稀释浓硫酸。副产物中的溴化氢可以用硝酸银溶液检验,但挥发的溴蒸气也会和硝酸银溶液生成白色沉淀,所以需要先除去溴蒸气。副产物中的乙醚(CH3CH2-O-CH2CH3)和产物CH3CH2Br都有乙基,不能通过红外光谱检验。除去溴乙烷中的杂质Br2,用NaOH溶液没有用NaHSO3溶液好,因为在NaOH溶液中溴乙烷会发生水解。
(二)溴乙烷难溶于水,和NaOH溶液分层,在NaOH溶液中发生水解后生成溶于水的乙醇,分层消失。若将溴乙烷和NaOH的乙醇溶液混合共热,溴乙烷会发生消去反应,生成乙烯,如果用酸性高锰酸钾检验生成的乙烯,必须先除去挥发的乙醇,乙烷乙醇也会使酸性高锰酸钾溶液褪色。
(1)仪器A的名称是三颈烧瓶;
(2)反应中加入少量的水,防止反应进行时发生大量的泡沫,减少副产物乙醚的生成和避免HBr 的挥发,故选abc。
(3)溴为橙红色液体,故此物质为溴。
(4)①检验溴化氢,可用硝酸银溶液或石蕊溶液检验,但先要除去混有的有机物,所以,将混合物通过有机溶剂,再通入硝酸银溶液或石蕊溶液。苯(或四氯化碳等有机溶剂)、硝酸银或石蕊试液。
②由于溴乙烷中也含乙基,故此同学的判断错误。
(5)除去溴乙烷中的少量杂质Br2,加NaI会引入碘单质杂质,a错误;加氢氧化钠会引起溴乙烷水解,b错误;加亚硫酸氢钠只与溴反应不与溴乙烷反应,c正确;加氯化钾都不反应;d错误。
(二)
(1)因为溴乙烷与氢氧化钠溶液不相溶,会出现分层,故液体不分层时,说明溴乙烷反应较完全。
(2)溴乙烷在NaOH乙醇溶液中反应,生成的气体混有乙醇蒸汽,所以将混合气体先通过水可除去乙醇。若无A试管,B试管中装高锰酸钾溶液,混合气体中的乙醇也可以使高锰酸钾褪色,故高锰酸钾要改为溴水。乙醇不与溴水反应。