题目内容
6.环境问题是现在社会急需解决的问题,有报道说:现在全球癌症的发病率呈上升趋势.有消息称:${\;}_{67}^{166}Ho$可有效地治疗肝癌,该原子核内的中子数与核外电子数之差为( )| A. | 67 | B. | 32 | C. | 99 | D. | 166 |
分析 根据原子符号的含义以及中子数=质量数-质子数,原子中核外电子数=核内质子数,据此分析解答.
解答 解:${\;}_{67}^{166}Ho$的质子数是67,质量数是166,中子数=质量数-质子数=166-67=99,原子中核外电子数=核内质子数=67,核内的中子数与核外的电子数之差为99-67=32,
故选:B.
点评 本题考查原子中的数量关系,掌握原子中质子数、质量数、中子数和核外电子数之间的关系是解本题的关键,难度不大.

练习册系列答案
 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
17.已知短周期元素的离子aA2+、bB+、cC2-、dD-都具有相同的核外电子排布,则下列叙述正确的是( )
| A. | 原子半径D<C<B<A | B. | 原子序数 d>c>a>b | ||
| C. | 离子半径C>D>B>A | D. | 单质的氧化性C>D>A>B |
11.下列各组顺序的排列错误的是( )
| A. | 离子半径:Na+>Mg2+>Al3+>F- | B. | 热稳定性:HCl>H2S>PH3>AsH3 | ||
| C. | 酸性:HAlO2<H2SiO3<H2CO3<H3PO4 | D. | 熔点:金刚石>NaCl>Na>CO2 |
18.学好化学用语是学好化学的基础,化学用语的书写必须十分规范与准确,请用化学用语回答下列问题:
(1)这10种元素中,化学性质最不活泼的元素是Ne,得电子能力最强的原子氢化物的分子式是HF,⑥元素最高价氧化物的电子式 ,④离子的核外电子排布示意图
,④离子的核外电子排布示意图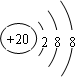 .
.
⑦、⑨两种元素最高价氧化物对应水化物的化学式分别为:H3PO4、HClO4;
⑦元素气态氢化物的稳定性小于⑨元素气态氢化物的稳定性(填大于、等于或小于)
(2)失电子能力最强的单质与水反应的化学方程式是2K+2H2O=2KOH+H2↑
(3)写出③的单质置换出⑥的单质的化学方程式2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
①和⑤两种元素最高价氧化物对应的水化物相互反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑧ | ⑩ | |||||
| 3 | ① | ③ | ⑤ | ⑦ | ⑨ | |||
| 4 | ② | ④ |
 ,④离子的核外电子排布示意图
,④离子的核外电子排布示意图 .
.⑦、⑨两种元素最高价氧化物对应水化物的化学式分别为:H3PO4、HClO4;
⑦元素气态氢化物的稳定性小于⑨元素气态氢化物的稳定性(填大于、等于或小于)
(2)失电子能力最强的单质与水反应的化学方程式是2K+2H2O=2KOH+H2↑
(3)写出③的单质置换出⑥的单质的化学方程式2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
①和⑤两种元素最高价氧化物对应的水化物相互反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O.
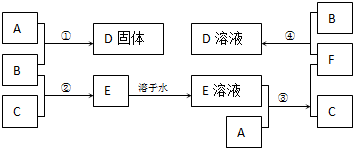 室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可以按下面的框图进行反应.又知E溶液是无色的.
室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可以按下面的框图进行反应.又知E溶液是无色的.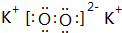 ;
;