题目内容
1.下列叙述中,正确的是( )| A. | 可将试管、蒸发皿、坩埚直接置于酒精灯火焰上加热 | |
| B. | 将二氧化硫通入到紫色石蕊试液中,试液先变红后褪色 | |
| C. | 用托盘天平称量氢氧化钠固体时,应将固体放在称量纸上 | |
| D. | 容量瓶在使用前用蒸馏水润洗,会影响所配制溶液的浓度 |
分析 A.试管、蒸发皿、坩埚可直接加热;
B.二氧化硫与水反应生成的亚硫酸能使石蕊试液变红,但二氧化硫不能使指示剂褪色;
C.易潮解或腐蚀性的药品,要放在玻璃器皿中称量;
D.分析操作对溶质的物质的量或对溶液的体积的影响.
解答 解:A.试管、蒸发皿、坩埚可置于酒精灯火焰上直接加热,故A正确;
B.二氧化硫与水反应生成的亚硫酸能使石蕊试液变红,但二氧化硫不能使指示剂褪色,所以变红后不褪色,故B错误;
C.氢氧化钠具有腐蚀性必须放在玻璃器皿中称量,故C错误;
D.最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响,故D错误.
故选A.
点评 本题考查常见仪器的使用和化学基本操作的方法,为高频考点,题目难度不大,注意在学习中加强基础知识的积累.

练习册系列答案
相关题目
11.${\;}_{27}^{69}$Co是放射性元素,它的核内中子数为( )
| A. | 60 | B. | 27 | C. | 33 | D. | 42 |
12.乙酸具有的官能团是( )
| A. | 碳碳双键 | B. | 羟基 | C. | 醛基 | D. | 羧基 |
9.正丁烷的一氯代物有几种( )
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
16.绿色化学提倡化工生产应提高原子利用率.在下列制备环氧乙烷的反应中,原子利用率最高的是( )
| A. | CH2=CH2+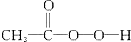 (过氧乙酸)→ (过氧乙酸)→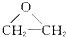 +CH3COOH +CH3COOH | |
| B. | CH2=CH2+Cl2+Ca(OH)2→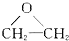 +CaCl2+H2O +CaCl2+H2O | |
| C. |  $\stackrel{催化剂}{→}$ $\stackrel{催化剂}{→}$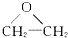 +HOCH2CH2-O-CH2CH2OH+2H2O +HOCH2CH2-O-CH2CH2OH+2H2O | |
| D. | 2CH2=CH2+O2$\stackrel{催化剂}{→}$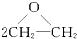 |
13.下列叙述错误的是( )
| A. | 吸热反应的反应物总能量低于生成物总能量 | |
| B. | 绿色植物进行光合作用时,将光能转化为化学能“贮存”起来 | |
| C. | 电力属于一次能源 | |
| D. | 物质的化学能可以在不同条件下转为热能、电能、光能等为人类所利用 |
10.在①钾盐 ②铵盐 ③硝酸盐 ④硫酸盐 ⑤盐酸盐 ⑥碳酸盐中,均能溶于水的一组盐是( )
| A. | ①②⑤ | B. | ②③④ | C. | ①②③ | D. | ①③⑥ |