题目内容

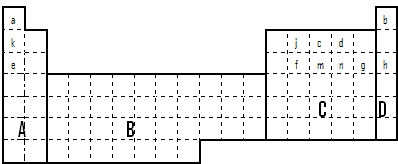
(1)在上面元素周期表中全部是金属元素的区域为
b
b
(a)A (b)B (c)C (d)D
(2)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或浓硝酸中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等.
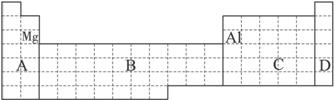
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置.
②甲、乙两元素相比较,金属性较强的是
Mg
Mg
(填名称),可以验证该结论的实验是
bc
bc
.(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
③写出甲的氧化物及氧化物对应水化物分别与强碱反应的离子方程式
Al2O3 +2OH-═2AlO2-+H2O
Al2O3 +2OH-═2AlO2-+H2O
、Al(OH)3 +OH-═AlO2-+2H2O
Al(OH)3 +OH-═AlO2-+2H2O
.(3)表中所列小写字母分别代表一种化学元素:
①m、f、j的单质熔点由高到低的顺序
C>Si>P
C>Si>P
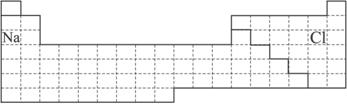
(填元素符号).②以上元素形成的金属单质中,熔点最低的是
Na
Na
(填元素符号).③f、m、n、g所形成的氢化物的稳定性还性由强到弱的顺序为
HCl、H2S、PH3、SiH4
HCl、H2S、PH3、SiH4
(填化学式);④甲、乙、c、d、e形成的简单离子的半径由小到大的顺序为
Al3+、Mg2+、Na+、O2-、N3-
Al3+、Mg2+、Na+、O2-、N3-
.⑤f元素单质是在生产中用量很大,试写出工业上制备f元素单质的化学方程式
SiO2+2C
2CO+Si
| ||
SiO2+2C
2CO+Si
.
| ||
⑥c元素的单质用途
氮气是合成氨、制硝酸的重要原料;由于其性质稳定常被用作保护气;在高科技领域中常用液氮制造低温环境
氮气是合成氨、制硝酸的重要原料;由于其性质稳定常被用作保护气;在高科技领域中常用液氮制造低温环境
(填一条).分析:(1)过渡元素均是金属元素;
(2)①根据元素的单质的性质和原子核外电子排布知识知识来推导元素,根据元素周期表的结构以及周期和族的划分来确定元素的位置;
②同周期从左到右,元素的单质金属性逐渐增强,和酸反应置换氢气的能力越强,和水反应越剧烈;
③氧化铝是两性氧化物,既能和强酸反应又能和强碱反应;
(3)①非金属元素,从上到下单质的熔点逐渐升高,从左到右单质的熔点逐渐降低;
②金属元素,从上到下单质的熔点逐渐降低,从左到右单质的熔点逐渐升高;
③同周期元素从左到右,氢化物的稳定性逐渐增强;
④核外电子数相同,则核内质子数越多半径越小;
⑤工业上用焦炭和石英反应来生产粗硅;
⑥氮气是一种重要的工业原料,化学性质稳定,可做保护气.
(2)①根据元素的单质的性质和原子核外电子排布知识知识来推导元素,根据元素周期表的结构以及周期和族的划分来确定元素的位置;
②同周期从左到右,元素的单质金属性逐渐增强,和酸反应置换氢气的能力越强,和水反应越剧烈;
③氧化铝是两性氧化物,既能和强酸反应又能和强碱反应;
(3)①非金属元素,从上到下单质的熔点逐渐升高,从左到右单质的熔点逐渐降低;
②金属元素,从上到下单质的熔点逐渐降低,从左到右单质的熔点逐渐升高;
③同周期元素从左到右,氢化物的稳定性逐渐增强;
④核外电子数相同,则核内质子数越多半径越小;
⑤工业上用焦炭和石英反应来生产粗硅;
⑥氮气是一种重要的工业原料,化学性质稳定,可做保护气.
解答:解:(1)在周期表中,所有的过渡元素均是金属元素,金属元素位于该图中的B区域,故答案为:b;
(2)①室温下,属于短周期的甲元素单质在冷的浓硫酸或浓硝酸中,表面都生成致密的氧化膜,只有金属铝符合要求,所以甲是Al,在第三周期第ⅢA族,原子核外M电子层与K电子层上的电子数相等的元素是Mg,在第三周期,第ⅡA族,故答案为: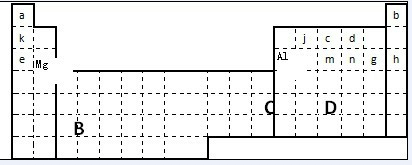 ;
;
②同周期从左到右,元素的单质金属性逐渐增强,所以金属镁的金属性较强,可以根据它们和酸反应置换氢气的快慢以及和水反应的剧烈剧烈程度或是看生成的氢氧化物的碱性的强弱,故答案为:Mg;bc;
③氧化铝是两性氧化物,既能和强酸反应又能和强碱反应,反应的实质是:Al2O3 +2OH-═2AlO2-+H2O;Al(OH)3 +OH-═AlO2-+2H2O;
(3)①根据元素周期表的结构和元素的分布,可知m、f、j分别是:P、Si、C,非金属元素,从上到下单质的熔点逐渐升高,从左到右单质的熔点逐渐降低,所以熔点由高到低的顺序为:C>Si>P,故答案为:C>Si>P;
②金属元素,从上到下单质的熔点逐渐降低,从左到右单质的熔点逐渐升高,所以以上元素形成的金属单质中,熔点最低的是Na,故答案为:Na;
③根据元素周期表的结构和元素的分布,可知f、m、n、g分别是:Si、P、S、Cl,同周期元素从左到右,氢化物的稳定性逐渐增强,即HCl>H2S>PH3>SiH4;
④根据元素周期表的结构和元素的分布,可知甲、乙、c、d、e形成的简单离子分别为:Al3+、Mg2+、N3-、O2-、Na+,它们核外电子数相同,则核内质子数越多半径越小,即离子的半径由小到大的顺序为:Al3+、Mg2+、Na+、O2-、N3-;
⑤工业上用焦炭和石英反应来生产粗硅,原理方程式为:SiO2+2C
2CO+Si,故答案为:SiO2+2C
2CO+Si;
⑥氮气是一种重要的工业原料,化学性质稳定,可做保护气,
故答案为:氮气是合成氨、制硝酸的重要原料(由于其性质稳定常被用作保护气;在高科技领域中常用液氮制造低温环境,任选一条回答).
(2)①室温下,属于短周期的甲元素单质在冷的浓硫酸或浓硝酸中,表面都生成致密的氧化膜,只有金属铝符合要求,所以甲是Al,在第三周期第ⅢA族,原子核外M电子层与K电子层上的电子数相等的元素是Mg,在第三周期,第ⅡA族,故答案为:
 ;
;②同周期从左到右,元素的单质金属性逐渐增强,所以金属镁的金属性较强,可以根据它们和酸反应置换氢气的快慢以及和水反应的剧烈剧烈程度或是看生成的氢氧化物的碱性的强弱,故答案为:Mg;bc;
③氧化铝是两性氧化物,既能和强酸反应又能和强碱反应,反应的实质是:Al2O3 +2OH-═2AlO2-+H2O;Al(OH)3 +OH-═AlO2-+2H2O;
(3)①根据元素周期表的结构和元素的分布,可知m、f、j分别是:P、Si、C,非金属元素,从上到下单质的熔点逐渐升高,从左到右单质的熔点逐渐降低,所以熔点由高到低的顺序为:C>Si>P,故答案为:C>Si>P;
②金属元素,从上到下单质的熔点逐渐降低,从左到右单质的熔点逐渐升高,所以以上元素形成的金属单质中,熔点最低的是Na,故答案为:Na;
③根据元素周期表的结构和元素的分布,可知f、m、n、g分别是:Si、P、S、Cl,同周期元素从左到右,氢化物的稳定性逐渐增强,即HCl>H2S>PH3>SiH4;
④根据元素周期表的结构和元素的分布,可知甲、乙、c、d、e形成的简单离子分别为:Al3+、Mg2+、N3-、O2-、Na+,它们核外电子数相同,则核内质子数越多半径越小,即离子的半径由小到大的顺序为:Al3+、Mg2+、Na+、O2-、N3-;
⑤工业上用焦炭和石英反应来生产粗硅,原理方程式为:SiO2+2C
| ||
| ||
⑥氮气是一种重要的工业原料,化学性质稳定,可做保护气,
故答案为:氮气是合成氨、制硝酸的重要原料(由于其性质稳定常被用作保护气;在高科技领域中常用液氮制造低温环境,任选一条回答).
点评:本题考查学生元素周期表和元素周期律的综合知识,要求学生具有分析和解决问题的能力,难度较大.

练习册系列答案
相关题目