题目内容
2.下列金属冶炼的反应原理,不正确的是( )| A. | 2NaCl(熔融)$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑ | B. | MgO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Mg+H2O | ||
| C. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | D. | 2Ag2O$\frac{\underline{\;\;△\;\;}}{\;}$4Ag+O2↑ |
分析 依据金属活泼性不同,金属冶炼的方法有:
电解法:冶炼活泼金属K、Ca、Na、Mg、Al,一般用电解熔融的氯化物(Al是电解熔融的三氧化二铝)制得;
热还原法:冶炼较不活泼的金属Zn、Fe、Sn、Pb、Cu,常用还原剂有(C、CO、H2等);
热分解法:Hg、Ag用加热分解氧化物的方法制得.据此解答.
解答 解:A.钠性质活泼用电解熔融氯化钠法制取,故A正确;
B.镁性质活泼应选择电解熔融氯化镁方法制取,故B错误;
C.铁性质较不活泼,用还原法制取,故C正确;
D.银性质稳定,用热分解氧化物的方法制取,故D正确;
故选:B.
点评 本题考查金属冶炼的一般方法和原理,熟悉金属的活泼性及采用相应的冶炼方法是解题关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.下列实验操作正确且能达到预期目的是( )
| 实验目的 | 操 作 | |
| ① | 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 |
| ② | 欲证明溶液中含有SO42- | 滴入盐酸酸化的硝酸钡溶液 |
| ③ | 欲证明溶液中含有S2- | 取少量溶液滴在醋酸铅试纸上看是否变黑 |
| ④ | 证明SO2具有漂白性 | 将SO2通入酸性KMnO4溶液中 |
| ⑤ | 比较确定铜和镁的金属活动性强弱 | 用Pt作电极电解Mg(NO3)2、Cu( NO3)2 混合液 |
| ⑥ | 确定碳和硅两元素非金属性强弱 | 测同温同浓度Na2CO3和Na2SiO3水溶液的PH |
| A. | ①⑤⑥ | B. | ②③⑤ | C. | ①④⑤ | D. | ①②③④⑤⑥ |
13.已知铅蓄电池的总反应为:Pb(s)+PbO2(s)+2H2SO4(aq) $?_{充电}^{放电}$2PbSO4(s)+2H2O(l)市场上一种手提应急灯,主要是“无液干粉”铅蓄电池,其原理是将浓硫酸灌注到硅胶凝胶中去,改善了电池的性能.下列说法不正确的是( )
| A. | 放电时,电子由Pb通过外电路转移到PbO2 | |
| B. | 充电时阴极反应:PbSO4+2e-=Pb(s)+SO42-(aq) | |
| C. | 充电时,电源的正极接铅蓄电池标“-”的一极 | |
| D. | “无液干粉”铅蓄电池中的电解质溶液不易发生泄漏 |
14.海水是宝贵的自然资源,将海水淡化与浓海水资源化结合起来是综合利用海水的重要途径之一.
(1)采用“空气吹出法”从浓海水吹出Br2,并用纯碱吸收,这样做的目的是使Br2富集;碱吸收溴的主要反应是Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3,吸收0.15mol Br2时,转移的电子为0.25mol.
(2)海水提镁的一段工艺流程如图:
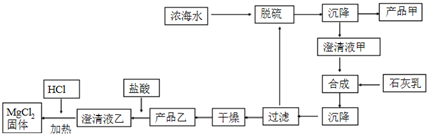
浓海水的主要成分如下:
①该工艺过程中,脱硫阶段主要的离子方程式为Ca2++SO42-=CaSO4↓,加入石灰乳时所发生的离子方程式是Mg2++Ca(OH)2=Mg(OH)2↓+Ca2+
②产品乙的化学式为Mg(OH)2,1L浓海水最多可得到产品乙的质量是69.9g.
(1)采用“空气吹出法”从浓海水吹出Br2,并用纯碱吸收,这样做的目的是使Br2富集;碱吸收溴的主要反应是Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3,吸收0.15mol Br2时,转移的电子为0.25mol.
(2)海水提镁的一段工艺流程如图:

浓海水的主要成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g•L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
②产品乙的化学式为Mg(OH)2,1L浓海水最多可得到产品乙的质量是69.9g.
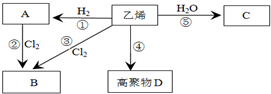 有机物A、B、C、D有如下转化关系.回答下列问题:
有机物A、B、C、D有如下转化关系.回答下列问题: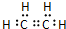 ,分子中含有的共价键类型有非极性键、极性键(填极性键或非极性键).
,分子中含有的共价键类型有非极性键、极性键(填极性键或非极性键). ,反应类型:加聚反应.
,反应类型:加聚反应.