��Ŀ����
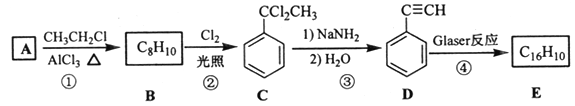
����Ŀ����Ȳ���ڴ��������¿ɷ���ż����Ӧ����ΪGlaser��Ӧ��2R��C��C��H![]() R��C��C��C��C��R+H2���÷�Ӧ���о����ͷ�����ϡ������ӻ�ѧ�ȷ��������Ҫ��ֵ������������Glaser��Ӧ�Ʊ�������E��һ�ֺϳ�·�ߣ�
R��C��C��C��C��R+H2���÷�Ӧ���о����ͷ�����ϡ������ӻ�ѧ�ȷ��������Ҫ��ֵ������������Glaser��Ӧ�Ʊ�������E��һ�ֺϳ�·�ߣ�
�ش��������⣺
��1��B�Ľṹ��ʽΪ______��D �Ļ�ѧ����Ϊ______��
��2���ٺ͢۵ķ�Ӧ���ͷֱ�Ϊ______��______��
��3��E�Ľṹ��ʽΪ______����1 mol E�ϳ�1,4���������飬��������Ҫ��������_______mol��
��4�������![]() ��Ҳ�ɷ���Glaserż����Ӧ���ɾۺ���þۺϷ�Ӧ�Ļ�ѧ����ʽΪ_____________________________________��
��Ҳ�ɷ���Glaserż����Ӧ���ɾۺ���þۺϷ�Ӧ�Ļ�ѧ����ʽΪ_____________________________________��
��5�����㻯����F��C��ͬ���칹�壬�������ֻ�����ֲ�ͬ��ѧ�������⣬��Ŀ��Ϊ3:1��д������3�ֵĽṹ��ʽ_______________________________��
��6��д����2�����Ҵ�Ϊԭ�ϣ��������Լ���ѡ���Ʊ�������D�ĺϳ�·��___________��
���𰸡� ![]() ����Ȳ ȡ����Ӧ ��ȥ��Ӧ
����Ȳ ȡ����Ӧ ��ȥ��Ӧ ![]() 4
4 


����������1��A�������鷢��ȡ����Ӧ����B�������B����ʽ��֪A�DZ���B�DZ����飬��B�Ľṹ��ʽΪ![]() ������D�Ľṹ��ʽ��֪D�Ļ�ѧ����Ϊ����Ȳ����2�����DZ�������ԭ�ӱ��һ�ȡ��������ȡ����Ӧ�����в���̼̼��������±��������ȥ��Ӧ����3��D������֪��Ϣ�ķ�Ӧ�����E�Ľṹ��ʽΪ
������D�Ľṹ��ʽ��֪D�Ļ�ѧ����Ϊ����Ȳ����2�����DZ�������ԭ�ӱ��һ�ȡ��������ȡ����Ӧ�����в���̼̼��������±��������ȥ��Ӧ����3��D������֪��Ϣ�ķ�Ӧ�����E�Ľṹ��ʽΪ![]() ��1��̼̼������Ҫ2���������ӳɣ�����1 molE�ϳ�1,4�����������飬��������Ҫ��������4mol����4��������֪��Ϣ��֪������
��1��̼̼������Ҫ2���������ӳɣ�����1 molE�ϳ�1,4�����������飬��������Ҫ��������4mol����4��������֪��Ϣ��֪������![]() ����Glaserż����Ӧ���ɾۺ���Ļ�ѧ����ʽΪ
����Glaserż����Ӧ���ɾۺ���Ļ�ѧ����ʽΪ![]() ����5�����㻯����F��C��ͬ���칹�壬�������ֻ�����ֲ�ͬ��ѧ�������⣬��Ŀ��Ϊ3:1���ṹ��ʽΪ
����5�����㻯����F��C��ͬ���칹�壬�������ֻ�����ֲ�ͬ��ѧ�������⣬��Ŀ��Ϊ3:1���ṹ��ʽΪ ����6���������Ʒ������֪��Ϣ�Լ��Ҵ������ʿ�֪��2�������Ҵ�Ϊԭ�ϣ��������Լ���ѡ���Ʊ�������D�ĺϳ�·��Ϊ
����6���������Ʒ������֪��Ϣ�Լ��Ҵ������ʿ�֪��2�������Ҵ�Ϊԭ�ϣ��������Լ���ѡ���Ʊ�������D�ĺϳ�·��Ϊ ��
��

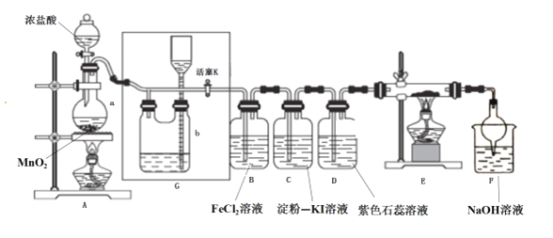
����Ŀ���������ֽ�ˮ�����������һ����Ҫ���л��ϳ�ԭ�ϡ�ij��ѧС����ˮ���ᣨ![]() ���ͼ״������Դ������ºϳ�ˮ�����������������ʡ�
���ͼ״������Դ������ºϳ�ˮ�����������������ʡ�
ʵ�鲽�裺
������ͼ����������ƿ�м���13.8g (0.1mol��ˮ�����24 g(30 mL��0.75 mol���״����������м���Լ10 mL�ױ�(�ױ���ˮ�γɵĹ�����е�Ϊ85������ʵ���м���ױ�����ˮ����������С�ĵؼ���5 mLŨ���ᣬҡ�����ȣ�����1��2����ʯ����װ��ʵ��װ�ã���85~95���º��¼��ȷ�Ӧ1.5Сʱ��
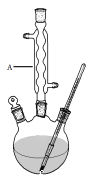
������װ����ȴ������״���Ȼ��ת������Һ©��������������ˮ��5%NaHCO3��Һ��ˮϴ�ӣ��ֳ��IJ������������ˮMgSO4���壬���˵õ�������
�������������������ռ�221����224������֣���ˮ�������9.12g��
��������������
���� | ������ | ��ɫ״̬ | ����ܶ� | �۵�(���� | �е�(���� |
ˮ������� | 152 | ��ɫҺ�� | 1.18 | -8.6 | 224 |
ˮ���� | 138 | ��ɫ���� | 1.44 | 158 | 210 |
�״� | 32 | ��ɫҺ�� | 0.792 | -97 | 64.7 |
�����������Ϣ�ش��������⣺
��1������A�������� �������ʯ�������� �������Ⱥ���δ�ӷ�ʯ��Ӧ��ȡ����ȷ������ ��
��2���Ʊ�ˮ�������ʱ������ʵļ��ȷ����� ��
��3��ʵ���м���ױ��Ժϳ�ˮ��������������� ��
��4����Ӧ����������״����õķ����� ��
��5��ʵ���м�����ˮ����þ�������� ��
��ʵ��IJ���Ϊ (������λ��Ч��������
����Ŀ��������ʵ����˵��Ԫ�صĽ����Ի�ǽ��������ǿ������
��� | ��ʵ | ���� |
A | ����ˮ��Ӧ��Na��Mg���� | �����ԣ�Na > Mg |
B | Ca(OH)2�ļ���ǿ��Mg(OH)2 | �����ԣ�Ca > Mg |
C | SO2��NaHCO3��Һ��Ӧ����CO2 | �ǽ����ԣ�S > C |
D | t��ʱ��Br2+H2 I2+H2 | �ǽ����ԣ�Br > I |
A. A B. B C. C D. D