题目内容
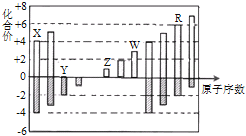
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y、W组成的一种化合物甲,25 ℃时,0.05 mol·L-1甲溶液中,![]() =1.0×l0l2;Z原子的最外层电子数是最内层电子数的
=1.0×l0l2;Z原子的最外层电子数是最内层电子数的![]() 。下列说法正确的是
。下列说法正确的是
A. 简单离子半径:Y<Z<W
B. Z分别与X、Y形成的化合物中,化学键类型均相同
C. X分别与Y、W形成的最简单化合物的稳定性:W<Y
D. 由以上四种元素形成的化合物一定能促进水的电离
【答案】C
【解析】0.05 mol·L-1甲溶液中![]() =1.0×l0l2可知此溶液为强酸溶液且为一元酸, 可知X为H、Y为O,Z原子的最外层电子数是最内层电子数的
=1.0×l0l2可知此溶液为强酸溶液且为一元酸, 可知X为H、Y为O,Z原子的最外层电子数是最内层电子数的![]() ,可知Z为Na,同时可知W为Cl;A.简单离子结构相同时核电荷数大,离子半径小,则Na+<O2-,故A错误;B.Na分别与H形成的NaH中只存在离子键,而Na与O形成的Na2O2中除离子键,还有非极性共价键,故B错误;C.非金属性越强,氢化物越稳定,氧的非金属性比氯强,则H分别与O、Cl形成的最简单化合物的稳定性HCl<H2O,故C正确;D.由以上四种元素形成的化合物NaClO因水解能促进水的电离,但NaClO4不水解,故D错误;答案为C。
,可知Z为Na,同时可知W为Cl;A.简单离子结构相同时核电荷数大,离子半径小,则Na+<O2-,故A错误;B.Na分别与H形成的NaH中只存在离子键,而Na与O形成的Na2O2中除离子键,还有非极性共价键,故B错误;C.非金属性越强,氢化物越稳定,氧的非金属性比氯强,则H分别与O、Cl形成的最简单化合物的稳定性HCl<H2O,故C正确;D.由以上四种元素形成的化合物NaClO因水解能促进水的电离,但NaClO4不水解,故D错误;答案为C。

 口算能手系列答案
口算能手系列答案【题目】用下图所示实验装置进行实验研究(图中a、b、c表示止水夹),请对其方案进行完善或评价。
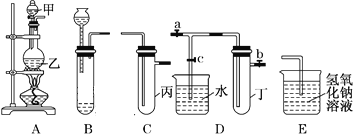
(1)实验室用装置A来制取Cl2,反应的离子方程式是______________;若将装置B、C、E相连后,用浓盐酸和______(填下列试剂的标号)为原料可制取Cl2。
a.KMnO4固体 b.KClO3固体 c.KCl固体 d.浓硫酸
(2)用装置B来制取制取氯气,并将装置B、C、E相连,在丙中加入适量水,即可制得氯水。向该氯水中加入大理石,充分振荡,观察到氯水的黄绿色逐渐褪去,同时产生少量气泡。某同学根据此现象推断出氯水呈酸性,请问该同学的推断是否合理?______________(填“合理”或“不合理”),若不合理,请说明理由(若合理,此空无需填写):_________________。
(3)为了探究氯水与大理石的反应,用装置A来制取氯气,并依次连接装置A、C、C、E。在第一个装置C的丙中,应加入的试剂是____________;在第二个装置C的丙中,加入适量水,即制得氯水。向制得的氯水中加入过量的大理石,反应结束后将所得溶液分成四等分,进行I、Ⅱ、Ⅲ、Ⅳ四个实验,实验操作如下,将实验现象或者实验结论填入下表:
实验序号 | 实验操作 | 实验现象 | 实验结论 |
Ⅰ | 将该溶液滴在有色布条上 | 有色布条迅速褪色 | ①该溶液中含有__________ |
Ⅱ | 向该溶液中滴加碳酸钠溶液 | ②___________ | 该溶液中含有Ca2+ |
Ⅲ | 向该溶液中滴加稀盐酸 | 有无色气泡产生 | ③无色气体是____________ |
Ⅳ | 加热该溶液 | 溶液变浑浊并产生大量气体 | ④该溶液中含有__________ |
⑤通过上述实验,得出氯水和过量的大理石反应的化学方程式为________________。