题目内容
【题目】焦亚硫酸钠![]() 是常用的食品抗氧化剂之一。某研究小组进行如下实验:
是常用的食品抗氧化剂之一。某研究小组进行如下实验:
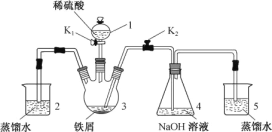
实验一:焦亚硫酸钠的制取。采用如图装置![]() 实验前已除尽装置内的空气
实验前已除尽装置内的空气![]() 制取
制取![]() 。装置Ⅱ中有
。装置Ⅱ中有![]() 晶体析出,发生的反应为
晶体析出,发生的反应为![]() 。
。

(1)A仪器的名称为: ______ ,实验前要进行 ______ ;装置Ⅰ中产生气体的化学方程式为 ______
(2)浓硫酸 ______ ![]() 能或不能
能或不能![]() 用稀硫酸代替,原因是 ______
用稀硫酸代替,原因是 ______
(3)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是 ______
(4)装置Ⅲ用于处理尾气,可选用如图的最合理装置![]() 夹持仪器已略去
夹持仪器已略去![]() 为 ______
为 ______ ![]() 填序号
填序号![]()
a.  b.
b.  c.
c.  d.
d. 
实验二:葡萄酒中抗氧化剂残留量的测定。
(5)葡萄酒常用![]() 作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量
作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量![]() 以游离
以游离![]() 计算
计算![]() 的方案如下:
的方案如下:
葡萄酒样品100.00mL![]() 馏分
馏分![]() 溶液出现蓝色且30s内不褪色
溶液出现蓝色且30s内不褪色![]() 已知:滴定时反应的化学方程式为
已知:滴定时反应的化学方程式为![]()
①按上述方案实验,消耗标准![]() 溶液
溶液![]() ,该次实验测得样品中抗氧化剂的残留量
,该次实验测得样品中抗氧化剂的残留量![]() 以游离
以游离![]() 计算
计算![]() 为 ______
为 ______ ![]()
②在上述实验过程中,若有部分HI被空气氧化,则测定结果 ______ ![]() 填“偏高”“偏低”或“不变”
填“偏高”“偏低”或“不变”![]() 。
。
【答案】分液漏斗 气密性检查 ![]() 浓
浓![]() 不能 二氧化硫易溶于水,故不能用稀硫酸 过滤 d
不能 二氧化硫易溶于水,故不能用稀硫酸 过滤 d ![]() 偏低
偏低
【解析】
(1)A仪器的名称为分液漏斗,实验前首先进行气密性检查;装置Ⅰ中浓硫酸与亚硫酸钠反应产生二氧化硫气体,同时生成硫酸钠和水,化学方程式:![]() 浓
浓![]() ,
,
故答案为:分液漏斗;气密性检查;![]() 浓
浓![]() ;
;
(2)稀硫酸不能代替浓硫酸,与亚硫酸钠反应产生的二氧化硫气体,易溶于水,故不能用稀硫酸,
故答案为:不能;二氧化硫易溶于水,使用稀硫酸时生成的SO2不易逸出;
(3)装置Ⅱ中析出![]() 晶体,通过过滤操作得到该晶体,故答案为:过滤;
晶体,通过过滤操作得到该晶体,故答案为:过滤;
(4)处理过量的![]() 尾气,a项装置瓶口封闭,错误;b项食盐水不能将大量的
尾气,a项装置瓶口封闭,错误;b项食盐水不能将大量的![]() 尾气吸收,错误;c项浓硫酸不能吸收二氧化硫,错误,d项氢氧化钠溶液可吸收
尾气吸收,错误;c项浓硫酸不能吸收二氧化硫,错误,d项氢氧化钠溶液可吸收![]() 尾气,同时能防倒吸,正确,故答案为:d;
尾气,同时能防倒吸,正确,故答案为:d;
(5)①根据反应“![]() ”,则样品中抗氧化剂的残留量
”,则样品中抗氧化剂的残留量![]() ,故答案为:0.16;
,故答案为:0.16;
②若有部分HI被空气氧化又生成![]() ,导致消耗标准
,导致消耗标准![]() 溶液的体积偏小,则测得结果偏低,故答案为:偏低。
溶液的体积偏小,则测得结果偏低,故答案为:偏低。

【题目】光纤通讯是光导纤维传送信号的一种通讯手段,合成光导纤维及氮化硅(一种无机涂层)的工艺流程如下:
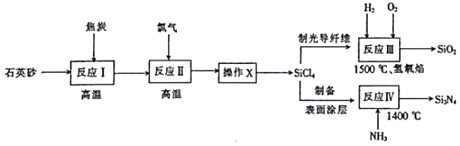
回答下列问题:
(1)反应Ⅰ的化学方程式为2C+SiO2 ![]() Si+2CO↑,其中还原剂为______,产物Si在周期表中位于______,该反应涉及的副反应可能有C+SiO2
Si+2CO↑,其中还原剂为______,产物Si在周期表中位于______,该反应涉及的副反应可能有C+SiO2 ![]() Si+CO2↑(碳不足)和______(碳足量)。
Si+CO2↑(碳不足)和______(碳足量)。
(2)经反应Ⅱ所得的四氯化硅粗品中所含的物质如下:
组分名称 |
|
|
| HCl |
|
|
质量分数 |
|
|
|
|
|
|
沸点 |
|
|
|
|
|
|
图中“操作X”的名称为______;![]() 的电子式为______。
的电子式为______。
(3)反应Ⅳ的化学方程式为3SiCl4+4NH3 ![]() Si3N4+12HCl,若向2L恒容密闭容器中投入1mol
Si3N4+12HCl,若向2L恒容密闭容器中投入1mol![]() 和1mol
和1mol![]() ,6min后反应完全,则
,6min后反应完全,则![]() min内,HCl的平均反应速率为______molL-lmin-l;反应Ⅲ的与Ⅳ产生的气体相同,则反应Ⅲ化学方程式为______。反应Ⅲ中的原料气
min内,HCl的平均反应速率为______molL-lmin-l;反应Ⅲ的与Ⅳ产生的气体相同,则反应Ⅲ化学方程式为______。反应Ⅲ中的原料气![]() 和
和![]() 在碱性条件下可构成燃料电池,其正极反应的电极方程式为______。
在碱性条件下可构成燃料电池,其正极反应的电极方程式为______。